��Ŀ����
��25��ʱ���ܱ�������X��Y��Z��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±���
|
���� |
X |
Y |
Z |
|
��ʼŨ��/mol��L-1 |
0.1 |
0.2 |
0 |
|
ƽ��Ũ��/mol��L-1 |
0.05 |
0.05 |
0.1 |
����˵���������
A����Ӧ�ﵽƽ��ʱ��X��ת����Ϊ50��
B����Ӧ�ɱ�ʾΪX��3Y 2Z����ƽ�ⳣ��ֵΪ1600
2Z����ƽ�ⳣ��ֵΪ1600
C������ѹǿʹƽ��������Z�ķ����ƶ���ƽ�ⳣ������
D���ı��¶ȿ��Ըı�˷�Ӧ��ƽ�ⳣ��
���𰸡�
A
��������
���������A��X��ת����Ϊ0.05/0.1��100%=50������ȷ��B���������ʵ�Ũ�ȱ仯��֮��Ϊ1:3:2����Ӧ�ɱ�ʾΪX��3Y 2Z����ƽ�ⳣ��ֵ
2Z����ƽ�ⳣ��ֵ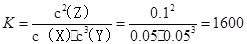 ����ȷ��C��ƽ�ⳣ��ֻ���¶��йأ�����D��ƽ�ⳣ��ֻ���¶��йأ��ı��¶ȿ��Ըı�˷�Ӧ��ƽ�ⳣ������ȷ��
����ȷ��C��ƽ�ⳣ��ֻ���¶��йأ�����D��ƽ�ⳣ��ֻ���¶��йأ��ı��¶ȿ��Ըı�˷�Ӧ��ƽ�ⳣ������ȷ��
���㣺����ת���ʡ�ƽ�ⳣ������Ӱ�����ء�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
��25��ʱ���ܱ�������X��Y��Z��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±���
|
��2009?���ϣ���25��ʱ���ܱ�������X��Y��Z��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±���
|
 2Z
2Z