��Ŀ����
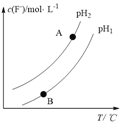
����Ŀ��������ͼ��ʾ��N2��g����O2��g����Ӧ����NO��g�������������仯������ж�����˵��������� �� ��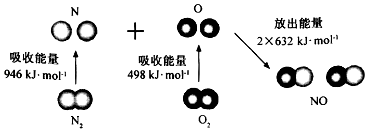
A.ֱ�ۿ����÷�Ӧ�з�Ӧ�������е����������������������е�������
B.2 mol��̬��ԭ�ӽ������O2��g��ʱ���ܷų�498 KJ����
C.����1 mol NO�����еĻ�ѧ������Ҫ����632KJ����
D.�÷�Ӧ���Ȼ�ѧ����ʽΪ��N2+O2�T2NO��H=+180KJ/mol��
���𰸡�D
���������⣺A���ʱ�=��Ӧ����ѻ�ѧ�����յ��������������γɻ�ѧ���ų���������N2+O2�T2NO��H=946kJ/mol+498kJ/mol��2��632kJ/mol=+180kJ/mol����Ӧ�����ȷ�Ӧ����Ӧ�з�Ӧ�������е����������������������е�����������A��ȷ�� B��1mol O2��g������498kJ�����γ�2mol Oԭ�ӣ�ԭ�ӽ���γɷ��ӵĹ����ǻ�ѧ���γɹ��̣��Ƿ��ȹ��̣�2mol Oԭ�ӽ������1mol O2��g��ʱ��Ҫ�ų�498kJ��������B��ȷ��
C���γ�2molNO����2��632KJ����������1mol NO��g�������еĻ�ѧ������ʱ��Ҫ����632kJ��������C��ȷ��
D���ʱ�=��Ӧ����ѻ�ѧ�����յ��������������γɻ�ѧ���ų���������N2+O2�T2NO��H=946kJ/mol+498kJ/mol��2��632kJ/mol=+180kJ/mol���Ȼ�ѧ����ʽ���۷�Ӧ�ﻹ���������������ۼ�״̬���ʱ����ֵ�ͷ���ʽ��ϵ�����Ӧ��ע���ʱ�ĵ�λ��kJ/mol�����Ը÷�Ӧ���Ȼ�ѧ����ʽΪ��N2��g��+O2��g���T2NO��g����H=+180KJ/mol����D����
��ѡD��
�����㾫����������Ŀ����֪���������÷�Ӧ�Ⱥ��ʱ�����֪ʶ���Եõ�����Ĵ𰸣���Ҫ�����ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�ȣ�

 ��Կ���Ծ�ϵ�д�
��Կ���Ծ�ϵ�д�����Ŀ���������ʵķ�����ȷ���ǣ� ��
ѡ�� | �� | �� | �� | ���������� |
A | �մ� | ���� | С�մ� | �������� |
B | ������ | ̼�� | ���� | һ������ |
C | �ռ� | ���� | ʯ��ʯ | �������� |
D | ���� | ���� | �⻯�� | һ����̼ |
A.AB.BC.CD.D