题目内容
【题目】用18mol/L 的浓硫酸配制 100mL 3.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释 ④检漏、转移、洗涤 ⑤定容、摇匀 回答下列问题:
(1)所需浓硫酸的体积是mL,量取浓硫酸所用的量筒的规格是(用下列编号填空). A.10mL B.25mL C.50mL D.100mL
(2)第③步实验的具体操作是
(3)第⑤步实 验 的 操 作 是 继 续 向 容 量 瓶 中 注 入 蒸 馏 水 至 离 刻 度 线 , 改用向容量瓶中滴加蒸馏水至为止.塞紧瓶塞,倒转摇匀并装试剂瓶.
(4)下列情况对所配制的稀硫酸浓度有何影响?(填“偏大”“偏小”或“无影响”)①所用的浓硫酸长时间放置在密封不好的容器中;
②容量瓶用蒸馏水洗涤后残留有少量的水;
③在转入容量瓶前烧杯中溶液未冷却至室温;
④加水超过刻度线后,用胶头滴管吸出多余的液体 .
【答案】
(1)16.7;B
(2)把16.7mL浓硫酸沿着烧杯内壁慢慢地注入水中,用玻璃棒不断搅拌
(3)1~2cm;胶头滴管;凹液面的最低处与刻度线相切
(4)偏小;无影响;偏大;偏小
【解析】解:(1)配制100ml 3.0mol/L 稀硫酸,需要18mol/L 浓硫酸的体积为: ![]() ≈0.0167L=16.7mL,量筒的选择方法为“近而大”,选择25mL量筒,所以答案是:16.7mL;B;(2)配制100ml 3.0mol/L 稀硫酸中,稀释浓硫酸为把 16.7 mL 浓硫酸沿着烧杯内壁慢慢地注入水中,用玻 璃棒不断搅拌,所以答案是:把 16.7 mL 浓硫酸沿着烧杯内壁慢慢地注入水中,用玻 璃棒不断搅拌;(3)定容操作为:继续向容量瓶注入蒸馏水至离刻度线1﹣2cm处,改用胶头滴管向容量瓶滴加至凹液面与刻度线相切,所以答案是:1﹣2cm;胶头滴管;凹液面与刻度线相切;(4)①.所用的浓硫酸长时间放置在密封不好的容器中,由于浓硫酸会吸水,导致浓硫酸的浓度偏小,所以答案是:偏小;②.容量瓶用蒸馏水洗涤后残留有少量的水,由于定容时还需要加入蒸馏水,所以不影响配制结果,所以答案是:无影响;③.在转入容量瓶前烧杯中溶液未冷却至室温,根据热胀冷缩的原理,体积减小,浓度偏大,所以答案是:偏大;④.加水超过刻度线后,用胶头滴管吸出多余的液体,造成溶质损失,浓度偏低,所以答案是:偏小.
≈0.0167L=16.7mL,量筒的选择方法为“近而大”,选择25mL量筒,所以答案是:16.7mL;B;(2)配制100ml 3.0mol/L 稀硫酸中,稀释浓硫酸为把 16.7 mL 浓硫酸沿着烧杯内壁慢慢地注入水中,用玻 璃棒不断搅拌,所以答案是:把 16.7 mL 浓硫酸沿着烧杯内壁慢慢地注入水中,用玻 璃棒不断搅拌;(3)定容操作为:继续向容量瓶注入蒸馏水至离刻度线1﹣2cm处,改用胶头滴管向容量瓶滴加至凹液面与刻度线相切,所以答案是:1﹣2cm;胶头滴管;凹液面与刻度线相切;(4)①.所用的浓硫酸长时间放置在密封不好的容器中,由于浓硫酸会吸水,导致浓硫酸的浓度偏小,所以答案是:偏小;②.容量瓶用蒸馏水洗涤后残留有少量的水,由于定容时还需要加入蒸馏水,所以不影响配制结果,所以答案是:无影响;③.在转入容量瓶前烧杯中溶液未冷却至室温,根据热胀冷缩的原理,体积减小,浓度偏大,所以答案是:偏大;④.加水超过刻度线后,用胶头滴管吸出多余的液体,造成溶质损失,浓度偏低,所以答案是:偏小.
【考点精析】根据题目的已知条件,利用配制一定物质的量浓度的溶液的相关知识可以得到问题的答案,需要掌握配制物质的量浓度溶液时,先用烧杯加蒸馏水至容量瓶刻度线1cm~2cm后,再改用交投滴管加水至刻度线.

【题目】纯净物根据其组成和性质可进行如下分类.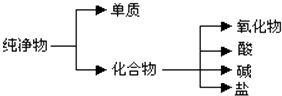
(1)如图所示的分类方法属于(填序号)
A.交叉分类法
B.树状分类法
(2)以H、O、S、N、K、Ba六种元素中任意两种或三种元素组成合适的常见物质,分别将其中一种常见物质的化学式填写于下表相应类别中:
物质类别 | 酸 | 碱 | 盐 | 氧化物 |
化学式 |
(3)从上表酸及碱中各选出一种能相互反应的物质,并写出其反应的化学方程式: .
