题目内容
|
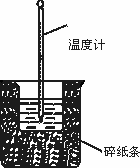
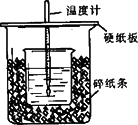
把 50 mL 1.0 mol/L的盐酸和50 mL 1.1 mol/L的NaOH溶液混合,若混合前两种溶液的温度均为24.4℃,而混合后溶液的温度变为31.2℃,设两种溶液的密度均为1 g/mL,混合液的比热容为4.18 J/(g·℃),则中和热为 | |
| [ ] | |
A. |
56.8 kJ/mol |
B. |
57.4 kJ/mol |
C. |
5.68 kJ/mol |
D. |
5.74 kJ/mol |
答案:A
解析:
解析:
|
|

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案
相关题目