题目内容
【题目】已知:CO2+Ca(OH)2![]() CaCO3↓+H2O,CaCO3+CO2+H2O
CaCO3↓+H2O,CaCO3+CO2+H2O![]() Ca(HCO3)2,且Ca(HCO3)2易溶于水。试根据如图所示装置回答下列问题:
Ca(HCO3)2,且Ca(HCO3)2易溶于水。试根据如图所示装置回答下列问题:
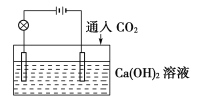
(1)通入CO2前,灯泡________(填“亮”或“不亮”)。
(2)开始通入CO2时,灯泡的亮度________。
(3)继续通入过量的CO2,灯泡的亮度________。
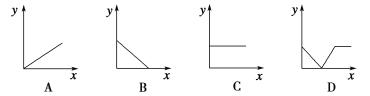
(4)下列四个图中,_______(填字母)能比较准确地反映出溶液的导电能力和通入CO2气体量的关系(x轴表示CO2通入的量,y轴表示导电能力)。
【答案】(1)亮
(2)先变暗后熄灭
(3)熄灭后又逐渐变亮
(4)D
【解析】(1)灯泡亮,因为Ca(OH)2溶于水后完全电离出离子,溶液中离子的浓度比较大,故灯泡亮。
(2)灯泡先变暗后熄灭,因为发生了CO2+Ca(OH)2![]() CaCO3↓+H2O,溶液中自由移动的离子减少。
CaCO3↓+H2O,溶液中自由移动的离子减少。
(3)灯泡熄灭后又逐渐变亮:CaCO3+CO2+H2O![]() Ca(HCO3)2,Ca(HCO3)2完全电离出自由移动的离子,溶液中离子浓度增大。
Ca(HCO3)2,Ca(HCO3)2完全电离出自由移动的离子,溶液中离子浓度增大。
(4)由于通入CO2后溶液中自由移动的离子的浓度逐渐减小,所以一开始导电能力逐渐下降,随着反应的进行,离子浓度逐渐增大,导电能力逐渐增大,所以选D。

 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案【题目】(1)立方氮化硼可利用人工方法在高温高压条件下合成,其硬度仅次于金刚石而远远高于其它材料,因此它与金刚石统称为超硬材料。BN的晶体结构与金刚石相似,其中B原子的杂化方式为__________,微粒间存在的作用力是__________。
(2)用“>”、“<”或“=”填写下列空格:
①沸点: H2S_______H2O ②酸性:H2SO4_______H2SeO4
③原子的核外电子排布中,未成对电子数:24Cr_______25Mn
④A、B元素的电子构型分别为ns2np3、 ns2np4, 第一电离能:A________B
(3)SiO2晶体结构片断如下图所示。SiO2晶体中:
Si原子数目和Si-O键数目的比例为_____________。
通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。
化学键 | Si-O | Si-Si | O=O |
键能/ KJ·mol-1 | 460 | 176 | 498 |

Si(s)+O2(g)![]() SiO2(s),该反应的反应热△H = ___________
SiO2(s),该反应的反应热△H = ___________
【题目】向1L含0.01molNaAlO2和0.02molNaOH的溶液中缓慢通入二氧化碳,随n(CO2)增大,先后发生三个不同的反应,当0.01mol<n(CO2) ![]() 0.015mol时发生的反应是:
0.015mol时发生的反应是:
2 NaAlO2+ CO2+2H2O=2Al(OH)3↓+Na2CO3。下列对应关系正确的是
选项 | n(CO2)/mol | 溶液中离子的物质的量浓度 |
A | 0 | c(Na+)>c(AlO2-)+c(OH-) |
B | 0.01 | c(Na+)>c(AlO2-)> c(OH-)>c(CO32-) |
C | 0.015 | c(Na+)> c(HCO3-)>c(CO32-)> c(OH-) |
D | 0.03 | c(Na+)> c(HCO3-)> c(OH-)>c(H+) |
A. A B. B C. C D. D