题目内容
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、1.8克金属铝变为铝离子时失去的电子数目为0.1NA |
| B、1.8克818O2中所含的中子数目为NA |
| C、在常温常压下11.2升氯气所含的原子数目为NA |
| D、氧气的摩尔质量与NA个O2分子的质量相同 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据n=
计算物质的量,结合铝原子结构分析计算失电子数;
B、依据n=
计算物质的量,结合质子数+中子数=质量数计算;
C、标准状况气体摩尔体积为22,4L/mol;
D、摩尔质量数值上等于相对分子质量.
| m |
| M |
B、依据n=
| m |
| M |
C、标准状况气体摩尔体积为22,4L/mol;
D、摩尔质量数值上等于相对分子质量.
解答:
解:A、依据n=
计算物质的量=
=,结合铝原子结构分析计算失电子数=
×3×NA=0.2NA,故A错误;
B、依据n=
计算物质的量=
=0.05mol,结合质子数+中子数=质量数计算,1.8克818O2中所含的中子数目=0.05mol(18-8)×2×NA=NA,故B正确;
C、标准状况气体摩尔体积为22,4L/mol,常温常压下11.2升氯气物质的量不是0.5mol,故C错误;
D、摩尔质量数值上等于相对分子质量,氧气的摩尔质量与NA个O2分子的质量单位不相同,故D错误;
故选B.
| m |
| M |
| 1.8g |
| 27g/mol |
| 1.8 |
| 27 |
B、依据n=
| m |
| M |
| 1.8g |
| 36g/mol |
C、标准状况气体摩尔体积为22,4L/mol,常温常压下11.2升氯气物质的量不是0.5mol,故C错误;
D、摩尔质量数值上等于相对分子质量,氧气的摩尔质量与NA个O2分子的质量单位不相同,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的分析应用,气体摩尔体积条件分析应用,注意摩尔质量和相对分子质量的概念理解区分,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
在同温同压下,一定量的某有机物和过量的金属钠反应产生a L氢气,另取等量的该有机物与足量的小苏打溶液反应,可以收集二氧化碳气体b L,若a=b,则该有机物可能是( )
| A、HOOC-COOH |
| B、HOOC-CH2CH2OH |
| C、HOCH2-CH2OH |
| D、CH3COOH |
下列金属中不属于货币金属的是( )
| A、铁 | B、金 | C、银 | D、铜 |
下列物质在常温下体积受压强影响最大的是( )
| A、水 | B、空气 | C、NaCl | D、酒精 |
下列说法正确的是( )
| A、CO2与CaO化合是放热反应,则CaCO3分解是吸热反应 |
| B、需要加热方能发生的反应一定是吸热反应 |
| C、若反应X+Y=M是放热反应,该反应一定不用加热 |
| D、1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热 |
下列关于煤和石油的说法正确的是( )
| A、煤和石油均属于可再生矿物能源 |
| B、煤经干馏再分馏可获得芳香烃 |
| C、石油分馏得到的各馏分均是纯净物 |
| D、石油裂解的目的是为了提高汽油的产量与质量 |
下列各组物质中,不管它们以何种比例混合,只要总物质的量一定,充分燃烧后消耗氧气的量一定的是( )
| A、C2H2和C6H6 |
| B、C2H6O和C3H6O2 |
| C、CH2O和C2H4O2 |
| D、C3H8和C4H8O2 |
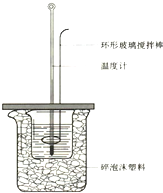 50mL 1.0mol?L-1盐酸跟50mL 1.1mol?L-1氢氧化钠溶液在如图装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:
50mL 1.0mol?L-1盐酸跟50mL 1.1mol?L-1氢氧化钠溶液在如图装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题: