题目内容
【题目】有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如图示的装置进行试验。通入二氧化硫气体,将带余烬的木条插入试管中,木条复燃。
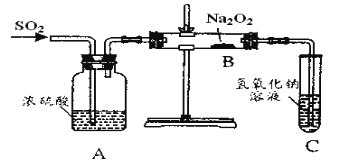
请回答下列问题:
(1)第一小组同学认为Na2O2与SO2反应生成的白色固体中含有Na2SO3和O2该反应的化学方程式为___。
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3___。
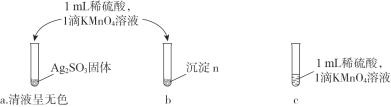
(3)第二小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案:
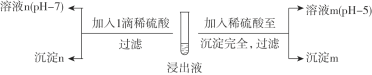
将B中反应后的固体溶解于水(再加BaCl2溶液)→白色沉淀→(加入稀硝酸)仍有部分白色沉淀不溶解,证明有Na2SO4生成。上述方案是否合理?___;请简要说明理由:__。
(4)在100mL混合溶液中,HNO3和H2SO4的物质的量浓度分别是0.4mol/L,0.1mol/L向该混合液中加入1.92g铜粉,加热待充分反应后,所得溶液中Cu2+的物质的量浓度是__(填选项字母)。
A.0.15 B.0.225 C.0.35 D.0.45
【答案】2Na2O2+2SO2=2Na2SO3+O2 取白色固体加入稀H2SO4,若产生能使品红溶液褪色的气体,则白色固体中含有Na2SO3 不合理 稀HNO3具有氧化性,可将BaSO3氧化成BaSO4(或者如果反应后的固体,它溶于水后能将亚硫酸根离子氧化成硫酸根离子) B
【解析】
(1)探究Na2O2与SO2的反应,由实验装置可知,浓硫酸干燥SO2,通入SO2气体,再用NaOH吸收尾气;
(2)可利用强酸制弱酸的反应原理检验Na2SO3,向反应后的溶液中滴加盐酸,再将生成的气体通入品红溶液中,若褪色则有SO2生成,原固体中含有Na2SO3;
(3)检验Na2SO4时,需排除Na2SO3的干扰,因为Na2SO3易被氧化成Na2SO4;硝酸、Na2O2氧化性均很强,均能将SO32-氧化成SO42-;
(4)Cu和HNO3、H2SO4构成的混合酸反应,可利用离子方程式计算。
(1)SO2与Na2O2反应生成Na2SO3和O2,化学方程式为2Na2O2+2SO2=2Na2SO3+O2;
(2)Na2SO3可与稀硫酸反应生成SO2,通过检验SO2来检验Na2SO3;实验操作为取白色固体加入稀H2SO4,若产生能使品红溶液褪色的气体,则白色固体中含有Na2SO3;
(3)SO32-能被硝酸氧化成SO42-,也能生成不溶于酸的白色沉淀;此外,反应中未反应完的Na2O2也具有强氧化性,也能氧化SO32-;答案为不合理,稀HNO3具有氧化性,可将BaSO3氧化成BaSO4(或者如果反应后的固体,它溶于水后能将亚硫酸根离子氧化成硫酸根离子);
(4)100mL混合溶液中,HNO3和H2SO4的浓度分别是0.4mol·L-1、0.1mol·L-1,则n(NO3-)=0.1L×0.4mol·L-1=0.04mol;n(H+)=0.1L×0.4mol·L-1+0.1L×0.1mol·L-1×2=0.06mol,1.92gCu的物质的量n(Cu)=![]() 。Cu和混合酸反应的离子方程式为3Cu+8H+2NO3-=3Cu2++2NO↑+4H2O,根据离子方程式可知,H+的量不足,根据H+的量计算。可得关系式8H+~3Cu2+,n(H+)=0.6mol,则n(Cu2+)=
。Cu和混合酸反应的离子方程式为3Cu+8H+2NO3-=3Cu2++2NO↑+4H2O,根据离子方程式可知,H+的量不足,根据H+的量计算。可得关系式8H+~3Cu2+,n(H+)=0.6mol,则n(Cu2+)=![]() ,则c(Cu2+)=
,则c(Cu2+)=![]() 。
。