题目内容
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述中正确的是( )
| A.离子半径:C>D>B>A | B.原子序数:d>c>b>a |
| C.原子半径:A>B>C>D | D.单质的还原性:A>B>D>C |
A
试题分析:aA2+、bB+、cC3-、dD-都具有相同电子层结构,则A、B在下一周期,为金属元素,且原子序数A>B,C、D在上一周期,为非金属元素,且原子序数D>C,A、具有相同电子排布的离子,原子序数大的离子半径小,原子序数为A>B>D>C,则离子半径为C3->D->B+>A2+,故A正确;B、由电子层数越多的原子序数越大,同周期从左向右原子序数在增大,所以原子序数为a>b>d>c,故B不正确;C、电子层越多,半径越大,同周期原子序数越大,半径越小,则原子半径为B>A>C>D,故C不正确;D、由同周期从左向右元素的金属性在减弱,非金属性在增强,金属性为B>A>C>D,则单质的还原性B>A>C>D,故D错误;故选BA。

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
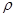 g·cm-3,阿伏加德罗常数为NA,求晶胞边长a= cm。(用含
g·cm-3,阿伏加德罗常数为NA,求晶胞边长a= cm。(用含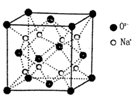
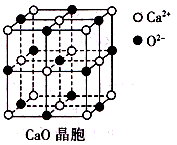
 ,每个晶胞中分摊2个钾原子
,每个晶胞中分摊2个钾原子 Rx[CrCln(H2O)6-n]+xH+。将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1NaOH溶液25.00 mL,则该配离子的化学式为_______。
Rx[CrCln(H2O)6-n]+xH+。将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1NaOH溶液25.00 mL,则该配离子的化学式为_______。