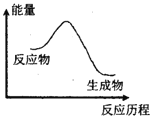
题目内容
【题目】下列各组物质中,满足表中图示物质在一定条件下一步转化关系的组合只有
序号 | X | Y | Z | W |
|
① | Cu | CuSO4 | Cu(OH)2 | CuO | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A.①②③B.①③④C.②③D.①④
【答案】A
【解析】
①Cu与浓硫酸反应生成CuSO4,再与NaOH反应生成Cu(OH)2,Cu(OH)2加热生成CuO,氢气还原CuO生成Cu;
②Na与水反应生成NaOH,再与二氧化碳反应生成Na2CO3,Na2CO3与盐酸反应生成NaCl,NaCl电解生成Na;
③Cl2与Ca(OH)2反应可生成Ca(ClO)2,盐酸酸性比次氯酸强,所以Ca(ClO)2中加入盐酸可生成次氯酸,HClO见光分解可生成HCl,浓HCl溶液与二氧化锰加热可生成氯气;
④Fe与氯气生成FeCl3,FeCl3与Fe反应FeCl2,FeCl2与NaOH反应生成Fe(OH)2,但Fe(OH)2不能一步转化为Fe。
①Cu![]() CuSO4
CuSO4![]() Cu(OH)2
Cu(OH)2![]() CuO
CuO![]() Cu,符合转化,故①正确;
Cu,符合转化,故①正确;
②Na![]() NaOH
NaOH![]() Na2CO3
Na2CO3![]() NaCl
NaCl![]() Na,符合转化,故②正确;
Na,符合转化,故②正确;
③Cl2![]() Ca(ClO)2
Ca(ClO)2![]() HClO
HClO![]() HCl,浓HCl溶液
HCl,浓HCl溶液![]() Cl2,转化均可实现,故③正确;
Cl2,转化均可实现,故③正确;
④Fe(OH)2不能一步转化为Fe,故④错误;
故答案为A。

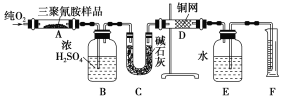
【题目】某化学小组同学用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件。供选试剂:30%H2O2溶液、0.1 mol/L H2SO4溶液、MnO2固体、KMnO4固体
(1)小组同学设计甲、乙、丙三组实验,记录如下(请补充完整甲组实验仪器的名称。)

操 作 | 现 象 | |
甲 | 向Ⅰ的锥形瓶中加入MnO2,向Ⅰ的________中加入30%的H2O2溶液,连接Ⅰ、Ⅲ,打开活塞 | Ⅰ中产生无色气体并伴随大量的白雾;Ⅲ中有气泡冒出,溶液迅速变蓝 |
乙 | 向Ⅱ中加入KMnO4固体,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液不变蓝 |
丙 | 向Ⅱ中加入KMnO4固体,Ⅲ中加入适量0.1mol/LH2SO4溶液,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液变蓝 |
(2)丙实验中O2与KI溶液反应的离子方程式是__________________。
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是____________。为进一步探究该条件对反应速率的影响,可采取的实验措施是____________。
(4)由甲、乙、丙三实验推测,甲实验可能是I中的白雾使溶液变蓝。学生将I中产生的气体直接通入下列_____________(填字母)溶液,证明了白雾中含有H2O2。
A.酸性 KMnO4 B. FeCl2 C. Na2S D.品红
(5)资料显示:KI溶液在空气中久置会被缓慢氧化:4KI+O2 +2H2O=2I2 +4KOH。该小组同学取20ml久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是:3I2+6OH-=5I-+IO3-+3H2O造成的。请设计实验证明他们的猜想是否正确:___。