题目内容
1.对于反应A+B═C+D,下列条件的改变一定使化学反应加快的是( )| A. | 增加A的物质的量 | B. | 升高体系的温度 | C. | 减少C的物质的量 | D. | 增加体系的压强 |
分析 A.增加A的物质的量反应速率不一定加快,如果A是固体或纯液体,则不影响反应速率;
B.升高温度,一定加快反应速率;
C.减少C的物质的量,不一定改变反应速率;
D.增加体系的压强,反应速率不一定加快.
解答 解:A.增加A的物质的量反应速率不一定加快,如果A是固体或纯液体,则不影响反应速率,故A错误;
B.升高温度,增大活化分子百分数导致反应速率一定加快,故B正确;
C.减少C的物质的量,如果C是固体或纯液体,C的物质的量不影响反应速率,如果C是气体或溶液,会导致反应速率降低,故C错误;
D.增加体系的压强,如果反应中没有气体,则压强不影响反应速率,故D错误;
故选B.
点评 本题考查化学反应速率影响因素,为高频考点,明确浓度、压强对反应速率影响的适用范围是解本题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.被誉为春果第一枝的大樱桃已经成为烟台农业经济的一个亮点.为了预防大樱桃在成熟期发生裂果现象,果农常施用一种钾肥.这种钾肥的水溶液能与氯化钡溶液反应生成不溶于硝酸的白色沉淀.该钾肥是( )
| A. | 硝酸钾 | B. | 碳酸钾 | C. | 硫酸钾 | D. | 氯化钾 |
12.某主族元素R的原子其电子式可用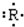 表示.该元素组成的以下物质,其分子式肯定错误的是( )
表示.该元素组成的以下物质,其分子式肯定错误的是( )
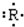 表示.该元素组成的以下物质,其分子式肯定错误的是( )
表示.该元素组成的以下物质,其分子式肯定错误的是( )| A. | 最高价氧化物分子式为R2O5 | B. | 含氧酸分子式为 HRO3 | ||
| C. | 含氧酸分子式为H3RO4 | D. | 气态氢化物分子式为RH5 |
9.关于元素周期表,下列叙述中不正确的是( )
| A. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 | |
| C. | 在金属元素区域可以寻找制备新型农药材料的元素 | |
| D. | 现有元素周期表包括18个纵列,共16个族 |
16.A、B、C、D、E五种元素的原子的原子序数都小于18,且具有相同的电子层,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序( )
| A. | B、A、D、C、E | B. | C、D、B、A、E | C. | B、A、C、D、E | D. | C、D、A、B、E |
6.图为反应2H2(g)+O2(g)═2H2O(g)的能量变化示意图.下列说法正确的是( )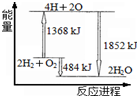

| A. | 拆开2molH2(g)和1mol O2(g)中的化学键成为H、O原子,共放出1368 kJ能量 | |
| B. | 由H、O原子形成2molH2O(g),共吸收1852kJ能量 | |
| C. | 2molH2(g)和1molO2(g)反应生成2molH2O(g),共吸收484 kJ能量 | |
| D. | 2molH2(g)和1molO2(g)反应生成2molH2O(g),共放出484 kJ能量 |
10.根据元素在周期表中位置,下列说法正确的是( )
| A. | 元素周期表金属和非金属交界处可以找到半导体材料 | |
| B. | Be(OH)2易溶于水 | |
| C. | Tl(OH)3一定是两性氢氧化物 | |
| D. | BaCO3是易溶于水的盐 |