题目内容
有关化学键和晶体的下列叙述中错误的是( )A.稀有气体的原子能形成分子晶体
B.金属晶体的熔沸点不一定很高
C.分子晶体中,分子间作用力越大分子越稳定
D.离子晶体中一定存在离子键
【答案】分析:A.稀有气体为单原子形成的分子;
B.金属晶体中有的熔点较高,有的较低,差别较大;
C.分子晶体的稳定性,与化学键有关;
D.离子晶体的作用力为离子键.
解答:解:A.稀有气体为单原子形成的分子,则属于分子晶体,故A正确;
B.金属晶体中有的熔点较高,有的较低,差别较大,且金属键的作用力一般小于离子键,所以金属晶体的熔沸点不一定很高,故B正确;
C.分子晶体的稳定性,与化学键有关,所以分子晶体中,分子间作用力越大,分子的熔沸点一般越大,不能确定分子的稳定性,故C错误;
D.离子晶体的构成微粒为离子,其作用力为离子键,故D正确;
故选C.
点评:本题考查化学键及晶体类型、晶体中的作用力,明确常见的晶体类型及其性质即可解答,注意稀有气体中不存在化学键,题目难度不大.
B.金属晶体中有的熔点较高,有的较低,差别较大;
C.分子晶体的稳定性,与化学键有关;
D.离子晶体的作用力为离子键.
解答:解:A.稀有气体为单原子形成的分子,则属于分子晶体,故A正确;
B.金属晶体中有的熔点较高,有的较低,差别较大,且金属键的作用力一般小于离子键,所以金属晶体的熔沸点不一定很高,故B正确;
C.分子晶体的稳定性,与化学键有关,所以分子晶体中,分子间作用力越大,分子的熔沸点一般越大,不能确定分子的稳定性,故C错误;
D.离子晶体的构成微粒为离子,其作用力为离子键,故D正确;
故选C.
点评:本题考查化学键及晶体类型、晶体中的作用力,明确常见的晶体类型及其性质即可解答,注意稀有气体中不存在化学键,题目难度不大.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
(1)下列有关晶体的叙述中错误的是
A.石英晶体中的硅原子以sp2杂化方式与周围的氧原子形成共价键
B.氯化钠晶体中每个Na+或Cl-周围紧邻的有6个Cl-或Na+
C.在CsCl晶体中每个Cs+周围紧邻的有8个Cl-,而和每个Cl-等距离紧邻的也有8个Cs+
D.在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子
(2)已知MgO的晶体结构属于NaCl型.某同学画出的MgO晶胞结构示意图如图1所示,请改正图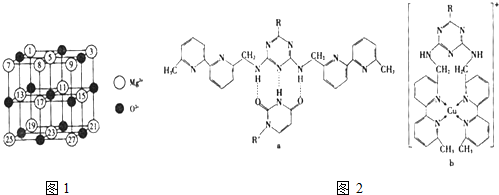
中错误: .(用文字表述)
(3)第三周期部分元素氟化物的熔点见下表:
解释表中氟化物熔点差异的原因: .
(4)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合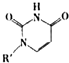 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b:
分析a和b中微粒间的相互作用(包括化学键和分子间相互作用)的差异,试指出
其不同点:a中含 ,b中含 .(用“氢键”、“配位键”、“极性键”、“非极性键”等填空)
A.石英晶体中的硅原子以sp2杂化方式与周围的氧原子形成共价键
B.氯化钠晶体中每个Na+或Cl-周围紧邻的有6个Cl-或Na+
C.在CsCl晶体中每个Cs+周围紧邻的有8个Cl-,而和每个Cl-等距离紧邻的也有8个Cs+
D.在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子
(2)已知MgO的晶体结构属于NaCl型.某同学画出的MgO晶胞结构示意图如图1所示,请改正图

中错误:
(3)第三周期部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1266 | 1534 | 183 |
(4)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合
 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b:分析a和b中微粒间的相互作用(包括化学键和分子间相互作用)的差异,试指出
其不同点:a中含
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题.
(1)砷原子核外电子排布式为______.
(2)K3[Fe(CN)6]晶体中Fe3-与CN-之间的键型为______,该化学键能够形成的原因是______.
(3)NH4+中氮原子的杂化类型为______,NH4+的空间构型为______.
(4)已知:
分析上表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是______;
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是______;
结合上述数据和规律判断,一定压强下HF和HC1的混合气体降温时______先液化.
(5)电负性(用X表示)也是元素的一种重要性质,下表给出8种元素的电负性数值:
请回答下列有关问题:
①估计钙元素的电负性的取值范围:______<X<______.
②经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AIC13中形成的化学键的类型及其理由是______.
(1)砷原子核外电子排布式为______.
(2)K3[Fe(CN)6]晶体中Fe3-与CN-之间的键型为______,该化学键能够形成的原因是______.
(3)NH4+中氮原子的杂化类型为______,NH4+的空间构型为______.
(4)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是______;
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是______;
结合上述数据和规律判断,一定压强下HF和HC1的混合气体降温时______先液化.
(5)电负性(用X表示)也是元素的一种重要性质,下表给出8种元素的电负性数值:
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 | 0.8 |
①估计钙元素的电负性的取值范围:______<X<______.
②经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AIC13中形成的化学键的类型及其理由是______.
 (2011?咸阳模拟)[化学-选修物质结构与性质]
(2011?咸阳模拟)[化学-选修物质结构与性质]