题目内容
【题目】![]() 时,含硫各微粒
时,含硫各微粒![]() 、
、![]() 图所示。下列说法不正确的是
图所示。下列说法不正确的是
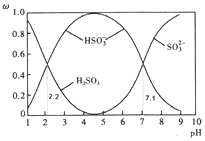
A.![]() 溶液显酸性
溶液显酸性
B.![]() 的溶液中不含
的溶液中不含![]()
C.在含![]()
![]() 、
、![]() 和
和![]() 的溶液中,加入少量NaOH固体,
的溶液中,加入少量NaOH固体,![]() 不一定增大
不一定增大
D.![]() 时,
时,![]()
![]()
【答案】B
【解析】
A.![]() 溶液中亚硫酸氢根离子水解平衡常数
溶液中亚硫酸氢根离子水解平衡常数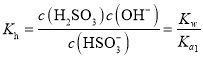 ,和
,和![]() 比较大小判断水解程度和电离程度大小;
比较大小判断水解程度和电离程度大小;
B.![]() 的溶液为亚硫酸钠溶液,亚硫酸根离子水解分步进行;
的溶液为亚硫酸钠溶液,亚硫酸根离子水解分步进行;
C.加入少量NaOH固体,![]() 可能增大也可能减小;
可能增大也可能减小;
D.![]() 时,
时,![]() ,结合电荷守恒分析判断离子浓度。
,结合电荷守恒分析判断离子浓度。
A.图象分析可知![]() ,
,![]() ,
,![]() 溶液中亚硫酸氢根离子水解平衡常数
溶液中亚硫酸氢根离子水解平衡常数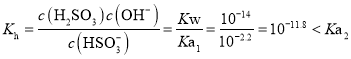 ,判断水解程度小于电离程度大小,溶液显酸性,故A不符合题意;
,判断水解程度小于电离程度大小,溶液显酸性,故A不符合题意;
B.![]() 的溶液为亚硫酸钠溶液,亚硫酸根离子水解分步进行,溶液中含
的溶液为亚硫酸钠溶液,亚硫酸根离子水解分步进行,溶液中含![]() ,故B符合题意;
,故B符合题意;
C.加入少量NaOH固体,若溶液中H2SO3较多,则随着溶液的pH增大,![]() 逐渐减小,
逐渐减小,![]() 逐渐增大,即
逐渐增大,即![]() 增大;若溶液中HSO3-较多,则HSO3-和OH-反应使
增大;若溶液中HSO3-较多,则HSO3-和OH-反应使![]() 降低,即
降低,即![]() 减小,故C不符合题意;
减小,故C不符合题意;
D.![]() 时,
时,![]() ,溶液中存在电荷守恒:
,溶液中存在电荷守恒:![]() ,
,![]() ,
,![]() ,故D不符合题意;
,故D不符合题意;
故选:B。

【题目】根据下列实验现象所得出的结论正确的是
选项 | 实验现象 | 实验结论 |
A | 将铝片分别投入浓、稀硝酸中,前者无明显现象,后者反应剧烈 | 稀硝酸的氧化性比浓硝酸的强 |
B | 滴有酚酞的Na2CO3溶液中加入BaCl2溶液,红色变浅 | Na2CO3溶液中存在水解平衡 |
C | 某溶液中滴加过量氨水产生白色沉淀且不溶解 | 该溶液中一定含有Mg2+ |
D | 溴水中通入SO2,溴水褪色 | SO2具有漂白性 |
A. A B. B C. C D. D
【题目】一定条件下对于可逆反应![]() ,若X、Y、Z三种气体的初始浓度和平衡浓度如下表(c1、c2、c3均不为零):
,若X、Y、Z三种气体的初始浓度和平衡浓度如下表(c1、c2、c3均不为零):
物质 | X | Y | Z |
初始浓度(mol·L-1) | c1 | c2 | c3 |
平衡浓度(mol·L-1) | 0.2 | 0.3 | 0.12 |
则下列判断正确的是( )
A.c1∶c2=2∶3
B.平衡时Y和Z的生成速率之比为2∶3
C.X、Y的转化率之比为2:3
D.c1的取值范围为0<c1<0.3