题目内容
设NA为阿伏加德罗常数的值,如果ag某气体双原子分子的分子数为p,则bg该气体在标准状况下的体积V(L)是( )

D
分子数是p,则该气体的物质的量是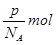 ,所以该气体的相对分子质量是
,所以该气体的相对分子质量是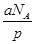 ,所以bg该气体的物质的量是
,所以bg该气体的物质的量是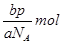 ,因此在标准状况下的体积是
,因此在标准状况下的体积是 ,答案选D。
,答案选D。
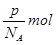 ,所以该气体的相对分子质量是
,所以该气体的相对分子质量是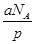 ,所以bg该气体的物质的量是
,所以bg该气体的物质的量是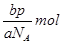 ,因此在标准状况下的体积是
,因此在标准状况下的体积是 ,答案选D。
,答案选D。
练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
题目内容

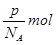 ,所以该气体的相对分子质量是
,所以该气体的相对分子质量是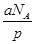 ,所以bg该气体的物质的量是
,所以bg该气体的物质的量是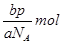 ,因此在标准状况下的体积是
,因此在标准状况下的体积是 ,答案选D。
,答案选D。
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案