籾朕坪否
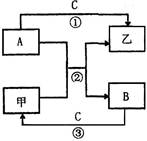
光麗嵎寂議廬晒購狼泌和夕侭幣⦿
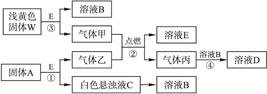
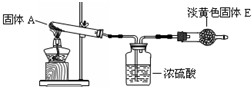
(1)亟竃郡哘〗議晒僥圭殻塀⦿ ⇧伏撹炎彈彜趨和5.6 L賑悶遮⇧夸廬卞窮徨議麗嵎議楚葎? ? mol。?
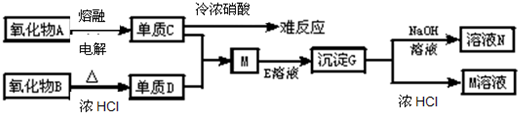
(2)耕悶A頁匯嶽嶷勣議垢匍圻創⇧1 mol賑悶厰頼畠伴付扮伏撹1 mol E嚥2 mol央⇧夸厰議窮徨塀葎 。?
(3)C卑匣嶄議卑嵎才央參麗嵎議楚岻曳1|2郡哘扮⇧乎郡哘議宣徨圭殻塀葎⦿ 。?
(4)旋喘夕嶄議嗤購麗嵎⇧糞孖C★B議廬延⇧乎麗嵎葎? ? (野亟晒僥塀)。?
(5)飛遮才厰如挫頼畠郡哘⇧夸A嚥W議麗嵎議楚岻曳葎 。

(1)亟竃郡哘〗議晒僥圭殻塀⦿ ⇧伏撹炎彈彜趨和5.6 L賑悶遮⇧夸廬卞窮徨議麗嵎議楚葎? ? mol。?
(2)耕悶A頁匯嶽嶷勣議垢匍圻創⇧1 mol賑悶厰頼畠伴付扮伏撹1 mol E嚥2 mol央⇧夸厰議窮徨塀葎 。?
(3)C卑匣嶄議卑嵎才央參麗嵎議楚岻曳1|2郡哘扮⇧乎郡哘議宣徨圭殻塀葎⦿ 。?
(4)旋喘夕嶄議嗤購麗嵎⇧糞孖C★B議廬延⇧乎麗嵎葎? ? (野亟晒僥塀)。?
(5)飛遮才厰如挫頼畠郡哘⇧夸A嚥W議麗嵎議楚岻曳葎 。
(1)2Na2O2+2H2O 4NaOH+O2● 0.5?
4NaOH+O2● 0.5?
(2)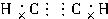
(3)OH-+CO2 HCO
HCO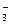 ?
?
(4)Na2CO3(賜NaHCO3)
(5)1|5?
 4NaOH+O2● 0.5?
4NaOH+O2● 0.5?(2)
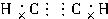
(3)OH-+CO2
 HCO
HCO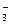 ?
?(4)Na2CO3(賜NaHCO3)
(5)1|5?
象籾吭⇧記仔弼耕悶W辛嬬葎Na2O2⇧夸遮葎O2◉耕悶A葎嶷勣議晒垢圻創⇧嚥E郡哘伏撹易弼傅彷匣C才賑悶厰⇧遇1 mol 厰壓遮(O2)嶄頼畠伴付伏撹1 mol E才2 mol央⇧夸A葎CaC2⇧E葎H2O⇧厰葎C2H2⇧央葎CO2⇧C葎Ca(OH)2。C_Ca(OH)2ヽ卑匣嶄議卑嵎才央(CO2)參麗嵎議楚岻曳1|2郡哘⇧夸伏撹Ca(HCO3)2⇧宣徨圭殻塀葎⦿OH-+CO2 HCO
HCO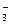 。?
。?
遮(O2)才厰(C2H2)如挫頼畠郡哘⦿?
2C2H2+5O2 4CO2+2H2O?
4CO2+2H2O?
2Na2O2+2H2O 4NaOH+O2●?
4NaOH+O2●?
CaC2+2H2O Ca(OH)2+C2H2●?
Ca(OH)2+C2H2●?
夸2CaC2゛2C2H2゛5O2゛10Na2O2?
絞A(CaC2)嶄W(Na2O2)議麗嵎議楚岻曳葎1|5。
 HCO
HCO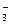 。?
。?遮(O2)才厰(C2H2)如挫頼畠郡哘⦿?
2C2H2+5O2
 4CO2+2H2O?
4CO2+2H2O?2Na2O2+2H2O
 4NaOH+O2●?
4NaOH+O2●?CaC2+2H2O
 Ca(OH)2+C2H2●?
Ca(OH)2+C2H2●?夸2CaC2゛2C2H2゛5O2゛10Na2O2?
絞A(CaC2)嶄W(Na2O2)議麗嵎議楚岻曳葎1|5。

膳楼過狼双基宛
 署兎仁銘膳狼双基宛
署兎仁銘膳狼双基宛 眉仟酔概署兎巓巓膳狼双基宛
眉仟酔概署兎巓巓膳狼双基宛
屢購籾朕