题目内容
6.(1)向CuSO4溶液中逐滴加入氨水,形成难溶物的原因是(请用离子方程式表示)Cu2++2NH3.H2O=Cu(OH)2+2NH4+.继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入乙醇,现象是有蓝色晶体生成.已知深蓝色物质是[Cu(NH3)4]2+,其结构可用示意图表示为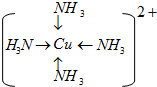 .
.(2)在BF3分子中,F-B-F的键角是120°.可溶于苯中,原因是BF3和苯都是非极性分子,根据相似相溶原理,BF3和过量NaF作用可生成NaBF4,BF4-的立体结构为正四面体;
(3)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键类型为极性共价键或共价键,层间作用力为分子间作用力或范德瓦耳斯力;
(4)立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有4个氮原子、4个硼原子,立方氮化硼的密度是\frac{25×4}{{({\;}\right.361.5×{{10}^{-10}}{{\left.{\;})}^3}×{N_A}}}g•cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA).
分析 (1)向CuSO4溶液中逐滴加入氨水,生成氢氧化铜沉淀,再加氨水可形成铜氨配合离子,沉淀溶解,若加入乙醇,乙醇能降低[Cu(NH3)4]SO4的溶解度;铜离子与配体氨分子形成配位键,据此写出其结构;
(2)在BF3分子中,B原子最外层价电子数对为3+32=3,所以B原子按sp2方式杂化,据此判断键角,根据相似相溶原理分析溶解性,BF3与F-通过配位键形成BF4-;
(3)石墨结构中层内碳原子之间以共价键作用,层间为分子间作用为,据此答题;
(4)根据金刚石的晶胞结构利用均摊法判断晶胞中原子数目,根据ρ=mV 计算密度.
解答 解:(1)向CuSO4溶液中逐滴加入氨水,生成氢氧化铜沉淀,反应的离子方程式为Cu2++2NH3.H2O=Cu(OH)2+2NH4+,再加氨水可形成铜氨配合离子,沉淀溶解,若加入乙醇,乙醇能降低[Cu(NH3)4]SO4的溶解度,溶液中有蓝色晶体生成;铜离子与配体氨分子形成配位键,其结构为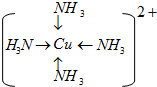 ,
,
故答案为:Cu2++2NH3.H2O=Cu(OH)2+2NH4+;有蓝色晶体生成;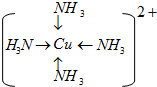 ;
;
(2)在BF3分子中,B原子最外层价电子数对为3+32=3,所以B原子按sp2方式杂化,所以F-B-F的键角是120°,BF3和苯都是非极性分子,根据相似相溶原理,BF3可溶于苯中,BF3与F-通过配位键形成BF4-,其结构与铵根离子相似,所以其立体结构为正四面体,
故答案为:120°;BF3和苯都是非极性分子,根据相似相溶原理;正四面体;
(3)石墨结构中层内碳原子之间以共价键作用,层间为分子间作用为,所以六方氮化硼晶体中,层内B原子与N原子之间的化学键类型为极性共价键或共价键,层间作用力为分子间作用力,
故答案为:极性共价键或共价键;分子间作用力;
(4)金刚石晶胞是立方体,其中8个顶点有8个碳原子,6个面各有6个碳原子,立方体内部还有4个碳原子,所以金刚石的一个晶胞中含有的碳原子数=8×18+6×12+4=8,因此立方氮化硼晶胞中应该含有4个N和4个B原子.一个晶胞中的质量为25gNA,一个立方氮化硼晶胞的体积是(361.5pm)3,因此立方氮化硼的密度是 \frac{25×4}{{({\;}\right.361.5×{{10}^{-10}}{{\left.{\;})}^3}×{N_A}}}g•pm-3,
故答案为:4;4; \frac{25×4}{{({\;}\right.361.5×{{10}^{-10}}{{\left.{\;})}^3}×{N_A}}}.
点评 本题考查较为全面,涉及到配合物的结构、配合物的形成以及有关晶体的计算,但解题具有较强的方法性和规律性,学习中注意基础知识和规律的应用,中等难度.

| A. | 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为(722.4)NA | |
| B. | 1mol羟基(-OH)所含的电子总数为10NA | |
| C. | 硝化甘油、火棉、TNT都是硝酸酯 | |
| D. | 1mol碳正离子(CH3+)所含的电子总数为8NA |
| 表述Ⅰ | 表述Ⅱ | |
| A | 在水中,NH3溶解度比I2的溶解度大 | NH3是极性分子,I2是非极性分子 |
| B | 通常条件下,HCl比HI稳定性高 | 非金属性:Cl>I |
| C | NH2OH中N的化合价为:-3 | 电负性:Cl>N |
| D | 沸点:SiO2>CO2 | 式量:SiO2>CO2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | CH4、C17H36 | B. | 醋酸CH3COOH、油酸C17H33COOH | ||
| C. | 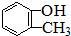 、 、 | D. | 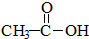 、 、 |
| A. | 往95%酒精中加入无水氯化钙,蒸馏得到无水乙醇 | |
| B. | 往2mL 10% CuSO4 溶液中滴加几滴2% NaOH,然后滴加少量乙醛,加热制得砖红色沉淀Cu2O | |
| C. | 用氯气和乙烷按1:1体积比混合,光照条件下,制纯一氯乙烷 | |
| D. | 往装有电石的烧瓶中逐滴滴加饱和食盐水,制粗乙炔 |
| A. | 蒸馏时,温度计水银球的位置应插入烧瓶的溶液中 | |
| B. | 配制溶液时,摇匀后发现液面低于刻度,加少量水至溶液凹液面恰好与刻度线相切 | |
| C. | 容量瓶用蒸馏水清洗后应烘干后使用 | |
| D. | 实验室制取蒸馏水时,冷凝管水流方向应从下到上,与蒸汽流动方向相反 |
| A. | 氯化钠溶液 | B. | 酒精 | C. | 硫酸钠晶体 | D. | 二氧化碳 |
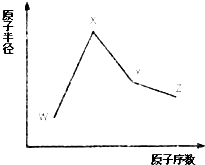 W、X、Y和Z是常见的短周期元素,其原子半径随原子序数变化如图所示.己知W的一种核素的质量数为18,中子数为10;X和Ne的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的原子半径在同周期主族元素中最小.
W、X、Y和Z是常见的短周期元素,其原子半径随原子序数变化如图所示.己知W的一种核素的质量数为18,中子数为10;X和Ne的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的原子半径在同周期主族元素中最小.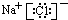 ;
;