题目内容
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.5.6 g铁粉在0.1 mol氯气中充分燃烧,转移电子数为0.3NA
B.1 mol Na2O2与足量H2O充分反应,转移的电子数为2NA
C.7.8 g Na2O2中含有的阴离子数等于0.1NA
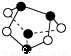
D.0.5 mol雄黄(As4S4,结构如下图)中含有NA个S—S键
C
【解析】5.6 g铁粉与0.1 mol氯气反应,铁粉过量,转移电子数为0.2NA,A项错误;Na2O2与水的反应为自身氧化还原反应,1 mol Na2O2与足量水反应转移电子数为NA,B项错误;Na2O2的阴离子为O22-,故7.8 g Na2O2所含的阴离子数为0.1NA,C项正确;从成键角度分析,黑球、白球分别为砷、硫,故0.5 mol雄黄中含NA个As—As键,不含S—S键,D项错误。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目