��Ŀ����
���ܱ������У����ڷ�Ӧ2SO2(g)��O2(g)  2SO3(g)��SO2��O2��ʼʱ�ֱ�Ϊ20mol��10 mol;��ƽ��ʱ��SO2��ת����Ϊ80%������SO3��ʼ���з�Ӧ������ͬ���¶��£���ʹƽ��ʱ���ɷֵİٷֺ�����ǰ����ͬ��������ʼʱSO3�����ʵ�������ת����Ϊ
2SO3(g)��SO2��O2��ʼʱ�ֱ�Ϊ20mol��10 mol;��ƽ��ʱ��SO2��ת����Ϊ80%������SO3��ʼ���з�Ӧ������ͬ���¶��£���ʹƽ��ʱ���ɷֵİٷֺ�����ǰ����ͬ��������ʼʱSO3�����ʵ�������ת����Ϊ
| A��10 mol�� 10% | B��20 mol�� 80% | C��20 mol�� 40% | D��20 mol�� 20% |
D
�����������������ͬ���¶��£�ʹƽ��ʱ���ɷֵİٷֺ�����ͬ��˵����ƽ���ǵ�Чƽ�⣬����ѧ����ת����һ�ߣ���Ӧ�ɷֵ����ʵ�����ͬ�����ݷ���ʽ2SO2��g��+O2��g��?2SO3��g����֪��20molSO2��10molO2��ȫת�����ɵ�n��SO3��=n��SO2��=20mol���ʴ�SO3��ʼ���з�Ӧ������ͬ��ƽ��״̬����ҪSO3�����ʵ���Ϊ20mol����SO2��O2��ʼ��ƽ��ʱ��SO2��ת����Ϊ80%SO2��ת����n��SO2��=20mol��80%=16mol������Ԫ���غ��֪��ƽ��ʱn��SO3��=n��SO2��=16mol�����Դ�SO3��ʼ���з�Ӧ������ͬ��ƽ��״̬��SO3�����ʵ�����ͬΪ16mol��ת����SO3�����ʵ���Ϊ20mol-16mol=4mol��SO3ת����Ϊ4/20=20%��
���㣺�����Чƽ��˼�롣

 ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д� ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д� ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д������й�˵����ȷ����
| A��Ǧ�����ڷŵ�ʱ���������������� |
| B��������������Һ����Ҫ�������ⸯʴ |
| C�������������Է����еķ�Ӧ�����Hһ��С��0 |
| D��0.1 mol��L��1Na2S��Һ��ˮϡ��ʱ��n(Na+)/n(S2��)ֵ����С |
һ�������£�ˮ���������淴Ӧʱ��ı仯���Ʒ�����ͼ����( )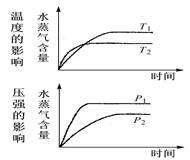
A��CO2(g)+2NH3( g) CO(NH2)2(s)+H2O(g); ��H<0 CO(NH2)2(s)+H2O(g); ��H<0 |
B��CO2(g)+ H2(g)  CO(g)+H2O(g); ��H>0 CO(g)+H2O(g); ��H>0 |
C��CH3CH2OH CH2=CH2(g)+ H2O(g); ��H>0 CH2=CH2(g)+ H2O(g); ��H>0 |
D��2C6H5CH2CH3(g)+O2(g) 2C6H-5CH=CH2(g)+2H2O(g); ��H<0 2C6H-5CH=CH2(g)+2H2O(g); ��H<0 |
������Ƭ��l00 mL 0.01 mol��L��ϡ���ᷴӦ����Ӧ����̫����Ϊ�˼ӿ�˷�Ӧ���ʶ����ı�H2�IJ���������ʹ�����·����е�
�ټ�H2O �ڼ�KNO3��Һ �۵��뼸��Ũ���� �ܼ����������� �ݼ�NaCl��Һ
���뼸������ͭ��Һ �������¶�(����������ӷ�) �����10 mL 0.1 mol��L����
| A���٢ޢ� | B���ۢݢ� | C���ۢߢ� | D���ۢܢޢߢ� |
�������ʶ���������Ʒ�Ӧ�ų�H2������H2������������ȷ����
��C2H5OH ��NaOH��Һ �۴�����Һ
| A���۩��ک��� | B���ک��٩��� | C���٩��ک��� | D���۩��٩��� |
����˵������ȷ����
| A������Ȼ���д��ڵĵ��ʣ�һ���߱���ѧ�����ȶ��������������ʷ�����Ӧ��һ���� |
| B��100����ǰ��Ӣ�����ľ��ʸĽ���¯����ͼ�ӳ�CO��Fe2O3�ĽӴ�ʱ�䣬�Լ���CO���ŷţ���Υ���˻�ѧ��Ӧ����һ������һ����ԭ�� |
| C������Һ�У���ɫ���ʲ���ķ�Ӧ�������÷ֹ��ȼ����ⶨ�仯ѧ��Ӧ���� |
| D����Ȼ̼��Ʒֽ���Ҫ���մ������ȣ����ڸ���������Ҳ���Է����� |
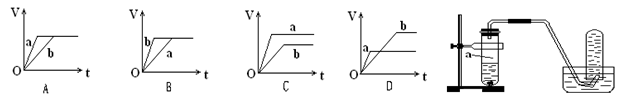
 2B��g����C��g����H��0����δ�ô������������Ѵ�ƽ�⣬��Ҫʹ����Ӧ���ʽ��ͣ�c��B����С��Ӧ��ȡ�Ĵ�ʩ��
2B��g����C��g����H��0����δ�ô������������Ѵ�ƽ�⣬��Ҫʹ����Ӧ���ʽ��ͣ�c��B����С��Ӧ��ȡ�Ĵ�ʩ��