题目内容
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | 85.5 | 115.2 | >600(分解) | 75.5 | 16.8 | 10.3 |
沸点/℃ | 60.3 | 444.6 | 10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子排布式为__________,基态S原子电子占据最高能级的电子云轮廓图为_________形,共有______能量不同的原子轨道;
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________。
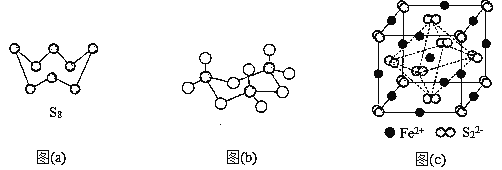
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为_______。
(4)气态H2S的分子的立体构型为_____形,固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3。
【答案】3d64s2 纺锤型 5 H2S S8与SO2都是分子晶体,S8相对分子质量比SO2大,S8的分子间作用力大于SO2,所以S8熔沸点比SO2高许多 V型 sp3杂化  (或
(或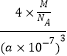 )
)
【解析】
(1)基态Fe原子价层电子为其3d、4s能级上电子;基态S原子电子占据的能级有1s、2s、2p、3s、3p,最高能级为3p,据此解答;
(2)根据价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=![]() (a-xb)依次计算H2S、SO2、SO3中S原子价层电子对个数后判断;
(a-xb)依次计算H2S、SO2、SO3中S原子价层电子对个数后判断;
(3)S8、SO2都分子晶体,分子晶体熔沸点与其分子间作用力成正比,据此分析解答;
(4)根据价层电子对互斥理论判断其空间构型;根据图示,该分子中每个S原子价层电子对个数都是4,根据价层电子对互斥理论判断S原子杂化类型;
(5)根据晶胞中微粒的计算方法,分别计算出Fe2+个数和S22-个数,再根据密度公式计算。
(1)基态Fe原子的电子排布式为[Ar]3d64s2;其中价电子排布式为3d64s2;基态S原子电子占据的能级有1s、2s、2p、3s、3p,最高能级为3p,其电子云轮廓图为哑铃形(或纺锤型),故答案为:3d64s2;哑铃形(或纺锤型);5;
(2)H2S中S原子价层电子对个数=2+![]() =4、SO2中S原子价层电子对个数=2+
=4、SO2中S原子价层电子对个数=2+![]() =3、SO3中S原子价层电子对个数=3+
=3、SO3中S原子价层电子对个数=3+![]() =3,中心原子价层电子对数不同于其他分子的是H2S,故答案为:H2S;
=3,中心原子价层电子对数不同于其他分子的是H2S,故答案为:H2S;
(3)S8、SO2都是分子晶体,分子晶体的熔沸点与其分子间作用力成正比,分子间作用力与其相对分子质量成正比,S8相对分子质量大于SO2,所以分子间作用力S8大于SO2,导致熔沸点S8大于SO2,故答案为:S8与SO2都是分子晶体,S8相对分子质量比SO2大,S8的分子间作用力大于SO2,所以S8熔沸点比SO2高许多;
(4)H2S中S原子价层电子对个数=2+![]() =4,H2S的分子的立体构型为V型;根据图示,固体三氧化硫中每个S原子价层电子对个数都是4,根据价层电子对互斥理论判断S原子杂化类型为sp3杂化,故答案为:V型;sp3杂化;
=4,H2S的分子的立体构型为V型;根据图示,固体三氧化硫中每个S原子价层电子对个数都是4,根据价层电子对互斥理论判断S原子杂化类型为sp3杂化,故答案为:V型;sp3杂化;
(5)晶胞边长为anm=a×10-7cm,晶胞体积=(a×10-7cm)3,该晶胞中Fe2+个数=1+12×![]() =4,S22-个数=8×
=4,S22-个数=8×![]() +6×
+6×![]() =4,其晶体密度=
=4,其晶体密度=![]() =
= g/cm3=
g/cm3= g/cm3,故答案为:
g/cm3,故答案为: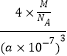 (或
(或 )。
)。