题目内容
在反应 3S + 6NaOH 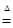 2Na2S + Na2SO3 + 3H2O 中被氧化的硫与被还原的硫的关系是 ( )
2Na2S + Na2SO3 + 3H2O 中被氧化的硫与被还原的硫的关系是 ( )
| A.物质的量之比为2∶1 | B.质量比为2∶1 |
| C.质量比为 1∶2 | D.物质的量之比为1∶1 |
C
解析正确答案:C
被氧化的硫与被还原的硫的关系就是化合价升高的硫与化合价降低的硫之比为1:2,由于都是同一物质,所以,物质的量之比为1:2,质量比也为 1∶2。

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
(10分,每空2分)(1)下列反应中属于氧化还原反应的是 。(填序号)
| A.MnO2 + 4HCl(浓)= MnCl2 + Cl2↑+ 2H2O | B.SO2+2H2S = 2H2O+3S↓ |
C.Ba(OH)2 + H2S O4 = BaSO4↓+2H2O O4 = BaSO4↓+2H2O | D.Cl2+2NaOH =" NaCl" +NaClO+H2O |
 4与浓盐酸发生如下反应:
4与浓盐酸发生如下反应:2KMnO4 + 16HCl(浓) ="==" 2KCl + 2MnCl2 + 5Cl2↑+8H2O。
在上述反应中,氧化剂是 。用单线桥法标出此反应的电子转移方向和数目。
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:
①将这6种物质分别填入下面对应的横线上,组成一个未配平的化学方程式:
________+________+H2SO4→ ________+________+________(填化学式)
②反应中1mol氧化剂得到______mol电子。