题目内容
【题目】钴(Co)是人体必需的微量元素。含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用。请回答下列问题:
(1)Co基态原子的价电子排布图为______;
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学疗法中的光敏剂、催化剂等方面得到了广泛的应用。其结构如图所示,中心离子为钴离子。
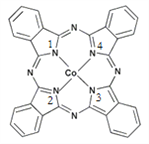
①酞菁钴中三种非金属原子的电负性由大到小的顺序为;______(用相应的元素符号作答);碳原子的杂化轨道类型为______;
②与钴离子通过配位键结合的氮原子的编号是______;
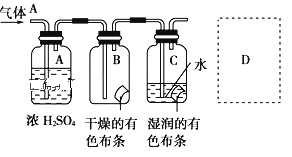
(3)CoCl2中结晶水数目不同呈现不同的颜色。
![]()
CoCl2可添加到硅胶(一种干燥剂,烘干后可再生反复使用)中制成变色硅胶。简述硅胶中添加CoCl2的作用________;
(4)用KCN处理含Co2+的盐溶液,有红色的Co(CN)2析出,将它溶于过量的KCN溶液后,可生成紫色的[Co(CN)6]4-,该配离子具有强还原性,在加热时能与水反应生成淡黄色[Co(CN)6]3-,写出该反应的离子方程式:________;
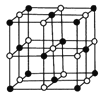
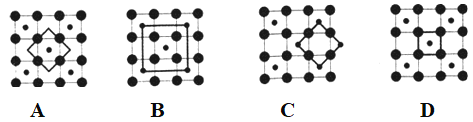
(5)Co的一种氧化物的晶胞如右图所示,在该晶体中与一个钴原子等距离且最近的钴原子有_________个;筑波材料科学国家实验室的一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是________。
【答案】 ![]() N>C>H sp2 2、4 随着硅胶的吸湿和再次烘干,二氯化钴在结晶水合物和无水盐间转化,通过颜色的变化可以表征硅胶的吸湿程度 2[Co(CN)6]4-+2H2O
N>C>H sp2 2、4 随着硅胶的吸湿和再次烘干,二氯化钴在结晶水合物和无水盐间转化,通过颜色的变化可以表征硅胶的吸湿程度 2[Co(CN)6]4-+2H2O![]() 2[Co(CN)6]3-+H2↑+2OH– 12 D
2[Co(CN)6]3-+H2↑+2OH– 12 D
【解析】(1)Co为27号元素,原子核外电子数为27,根据能量最低原理,其核外电子排布式为:1s22s22p63s23p63d74s2,价电子排布图为![]() ,故答案为:
,故答案为:![]() ;
;
(2)①酞菁钴中三种非金属原子为C、N、H,同周期自左而右电负性增大,非金属性越强电负性越大,故电负性N>C>H;分子中C原子均形成3个σ键,没有孤对电子,杂化轨道数目为3,碳原子的杂化轨道类型为 sp2,故答案为:N>C>H;sp2;
②含有孤对电子的N原子与Co通过配位键结合,形成配位键后形成4对共用电子对,形成3对共用电子对的N原子形成普通的共价键,1号、3号N原子形成3对共用电子对为普通共价键,2号、4号N原子形成4对共用电子对,与Co通过配位键结合,故答案为:2,4;
(3)随着硅胶的吸湿和再次烘干,二氯化钴在结晶水合物和无水盐间转化,通过颜色的变化可以表征硅胶的吸湿程度,故答案为:随着硅胶的吸湿和再次烘干,二氯化钴在结晶水合物和无水盐间转化,通过颜色的变化可以表征硅胶的吸湿程度;
(4)[Co(CN)6]4-配离子具有强还原性,在加热时能与水反应生成淡黄色[Co(CN)6]3-,只能是水中氢元素被还原为氢气,根据电荷守恒有氢氧根离子生成,该反应离子方程式为:2[Co(CN)6]4-+2H2O![]() 2[Co(CN)6]3-+H2↑+2OH -,故答案为:2[Co(CN)6]4-+2H2O
2[Co(CN)6]3-+H2↑+2OH -,故答案为:2[Co(CN)6]4-+2H2O![]() 2[Co(CN)6]3-+H2↑+2OH -;
2[Co(CN)6]3-+H2↑+2OH -;
(5)由氧化物晶胞结构可知晶胞中Co、O原子数目之比为1:2,假设黑色球为Co原子,以顶点Co原子为研究对象,与之等距离且最近的钴原子位于面心,每个顶点为8个晶胞共用,每个面心为2个晶胞共用,在该晶体中与一个钴原子等距离且最近的钴原子数目为![]() =12;CoO2的重复结构单元示意图中Co、O原子数目之比应为1:2,由图像可知:
=12;CoO2的重复结构单元示意图中Co、O原子数目之比应为1:2,由图像可知:
A中Co、O原子数目之比为1:4×![]() =1:2,符合,B中Co、O原子数目之比为(1+4×
=1:2,符合,B中Co、O原子数目之比为(1+4×![]() ):4=1:2,符合,C中Co、O原子数目之比为4×
):4=1:2,符合,C中Co、O原子数目之比为4×![]() :4×
:4×![]() =1:2,符合,D中Co、O原子数目之比为1:4×
=1:2,符合,D中Co、O原子数目之比为1:4×![]() =1:1,不符合,故答案为:12;D。
=1:1,不符合,故答案为:12;D。

 阅读快车系列答案
阅读快车系列答案