题目内容
如图所示曲线表示其它条件一定时反应2NO(g)+O2(g) 2NO2(g) △H<0,NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达平衡状态且V(正)>V(逆)的点是
2NO2(g) △H<0,NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达平衡状态且V(正)>V(逆)的点是
| A.a点 | B.b点 | C.c 点 | D.d点 |
C
解析试题分析:在曲线上,当温度一定时,NO的转化率也一定,故曲线上任意一点都表示达到平衡状态,而曲线外的任意一点都表示未达平衡状态。在曲线下方的任意一点,要想达到同温度下的平衡状态,应该向上引垂直线到曲线上的一点,这样NO的转化率要增大,平衡向右移动;而在曲线上方的任意一点,要想达到同温度下的平衡状态,则应该向下引垂直线到曲线上的一点,这样NO的转化率要减小,平衡向左移动,据此解答。A、a点在曲线上,处于平衡状态,v(正)=v(逆),故A错误;B、b点在曲线上,处于平衡状态,v(正)=v(逆),故B错误;C、c点在曲线下方,未达到平衡状态,要想达到同温度下的平衡状态,需要由c点向上引垂直线到曲线上的一点,这样NO的转化率要增大,平衡向右移动,故v(正)>v(逆),因此C正确;D、d点在曲线上方,未达到平衡状态,要想达到同温度下的平衡状态,需要由d点向下引垂直线到曲线上的一点,这样NO的转化率要减小,平衡向左移动,故v(正)<v(逆),因此D错误,答案选C。
考点:考查平衡状态的判断、可逆反应图像识别以及外界条件对平衡状态的影响等

 阅读快车系列答案
阅读快车系列答案下列说法正确的是
| A.增大体系压强,活化分子数增加,化学反应速率一定增大 |
| B.加入反应物,使活化分子百分数增加,化学反应速率增大 |
| C.活化分子间所发生的分子间的碰撞均为有效碰撞 |
| D.升高温度,活化分子百分数增加,化学反应速率一定增大 |
化学平衡常数(K)是化学反应限度的一个重要参数,该常数表示的意义是可逆反应进行的程度,K值越大,表示的意义错误的是( )
| A.温度越高 | B.反应物浓度越小 |
| C.反应进行的越完全 | D.生成物浓度越大 |
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
A.反应CO(g)+H2O(g) CO2(g)+H2(g)的△H>0 CO2(g)+H2(g)的△H>0 |
| B.在T2时,若反应进行到状态D,则一定有v正<v逆 |
| C.平衡状态A与C相比,平衡状态A的c(CO)小 |
| D.由D状态转变为C状态后,混合气体的平均相对分子质量不变 |
下列各组Na2S2O3溶液跟稀H2SO4反应的实验中,溶液中最先变浑浊的是
| 选项 | 反应 温度 | 反 应 物 | H2O | |||
| Na2S2O3 | H2SO4 | |||||
| t(℃) | V(mL) | c(mol×L-1) | V(mL) | c(mol×L-1) | V(mL) | |
| A | 10 | 5 | 0.1 | 10 | 0.1 | 10 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | 30 |
| C | 30 | 5 | 0.1 | 5 | 0.1 | 10 |
| D | 30 | 5 | 0.2 | 5 | 0.2 | 35 |
已知反应:2SO2(g)+O2(g)  2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是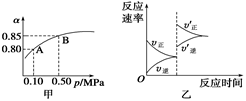
| A.由图甲知,A点SO2的平衡浓度为0.4 mol/L |
| B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2 |
| C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
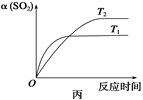
| D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
某温度下,某容积恒定的密闭容器中发生如下可逆反应:
CO(g)+H2O(g) H2(g)+CO2(g)△H>0。当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
H2(g)+CO2(g)△H>0。当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
| A.升高温度 | B.加入催化剂 |
| C.再加入n molCO和n molH2O | D.再加入2n molCO2和2n molH2 |
 2B(g)+C (g),下列能说明反应已达平衡状态的是
2B(g)+C (g),下列能说明反应已达平衡状态的是 xC(g),达平衡后,C在平衡混合气中的体积分数为w。若维持温度不变,按1.2molA、0.4molB、0.6molC为起始物质,达平衡后压强不变,C的体积分数仍为w,则x的值为
xC(g),达平衡后,C在平衡混合气中的体积分数为w。若维持温度不变,按1.2molA、0.4molB、0.6molC为起始物质,达平衡后压强不变,C的体积分数仍为w,则x的值为