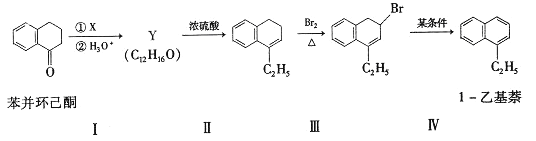
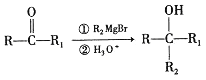
题目内容
【题目】一定温度时,向2.0 L恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:
2SO2(g)+O2(g) ![]() 2SO3(g)。经过一段时间后达到平衡。反应过程中测定部分数据见下表:
2SO3(g)。经过一段时间后达到平衡。反应过程中测定部分数据见下表:
t / s | 0 | 2 | 4 | 6 | 8 |
n(SO3) / mol | 0 | 0. 8 | 1. 4 | 1.8 | 1.8 |
下列说法正确的是
A. 反应在前2 s 的平均速率v(O2) = 0. 4 mol·L-1·s-1
B. 保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C. 保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2)增大
D. 相同温度下,起始时向容器中充入4 mol SO3,达到平衡时,SO3的转化率大于10%
【答案】C
【解析】A.根据表格中数据知,当n(SO3)=1.8mol,该反应达到平衡状态,反应在前2s的平均速率v(SO3)= 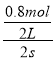 =0.2molL-1s-1,同一可逆反应中同一段时间内各物质的反应速率之比等于其计量数之比,v(O2)=
=0.2molL-1s-1,同一可逆反应中同一段时间内各物质的反应速率之比等于其计量数之比,v(O2)= ![]() ×0.2molL-1s-1=0.1molL-1s-1,故A错误;B.化学平衡常数只与温度有关,温度不变,化学平衡常数不变,与压强、物质浓度都无关,故B错误;C.温度不变,向该容器中再充入2molSO2、1molO2,增大了压强,平衡正向移动,三氧化硫的物质的量增加,氧气的物质的量减小,所以比值增大,故C正确;D.相同温度下,起始时向容器中充入4molSO3,如果三氧化硫完全转化为二氧化硫和氧气,二氧化硫和氧气的物质的量分别是4mol、2mol,为原来的2倍,增大压强平衡正向移动,则二氧化硫转化率增大,所以二氧化硫转化率大于90%,相同温度下,起始时向容器中充入4molSO3,达到平衡时,SO3的转化率小于10%,故D错误;故选C。
×0.2molL-1s-1=0.1molL-1s-1,故A错误;B.化学平衡常数只与温度有关,温度不变,化学平衡常数不变,与压强、物质浓度都无关,故B错误;C.温度不变,向该容器中再充入2molSO2、1molO2,增大了压强,平衡正向移动,三氧化硫的物质的量增加,氧气的物质的量减小,所以比值增大,故C正确;D.相同温度下,起始时向容器中充入4molSO3,如果三氧化硫完全转化为二氧化硫和氧气,二氧化硫和氧气的物质的量分别是4mol、2mol,为原来的2倍,增大压强平衡正向移动,则二氧化硫转化率增大,所以二氧化硫转化率大于90%,相同温度下,起始时向容器中充入4molSO3,达到平衡时,SO3的转化率小于10%,故D错误;故选C。

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案【题目】某学习小组研究溶液中Fe2+的稳定性,进行如下实验,观察,记录结果。

实验Ⅰ
物质 | 0 min | 1min | 1h | 5h |
FeSO4 | 淡黄色 | 桔红色 | 红色 | 深红色 |
(NH4)2Fe(SO4)2 | 几乎无色 | 淡黄色 | 黄色 | 桔红色 |
(1)上述(NH4)2Fe(SO4)2溶液pH小于FeSO4的原因是________________(用化学用语表示)。溶液的稳定性:FeSO4_______(NH4)2Fe(SO4)2(填“>”或“<”) 。
(2)甲同学提出实验Ⅰ中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+具有还原性。进行实验Ⅱ,否定了该观点,补全该实验。
操作 | 现象 |
取________________________, 滴加__________________,观察。 | 与实验Ⅰ中(NH4)2Fe(SO4)2溶液现象相同。 |
(3)乙同学提出实验Ⅰ中两溶液的稳定性差异是溶液酸性不同导致,进行实验Ⅲ:分别配制0.80 mol·L-1 pH为1、2、3、4的FeSO4溶液,观察,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短。
资料显示:亚铁盐溶液中存在反应4Fe2++O2+10H2O ![]() 4Fe(OH)3+8H+
4Fe(OH)3+8H+
由实验III,乙同学可得出实验的结论是____________,原因是______________________。

(4)进一步研究在水溶液中Fe2+的氧化机理。测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如图(实验过程中溶液温度几乎无变化)。反应初期,氧化速率都逐渐增大的原因可能是______________。
(5)综合以上实验,增强Fe2+稳定性的措施有_________________。
(6)向溶液中加入一定量H2O2氧化Fe2+。为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,离子方程式如下:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2
①在向滴定管注入K2Cr2O7标准溶液前,滴定管需要检漏、_________ 和_______________。
②若滴定xmL滤液中的Fe2+,消耗amol·L—1K2Cr2O7标准溶液bmL,则滤液中c(Fe2+)= ___________mol·L-1