题目内容
(10分)红磷 P (s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g)。如图所示(图中的△H表示生成 l mol 产物的数据)。
根据上图回答下列问题:
(1)P和CI2反应生成 PC13的热化学方程式是______________________________;
(2)PC15分解成 PC13和 Cl2的热化学方程式是_____________________________;上述分解反应是一个可逆反应。温度 Tl时,在密闭容器中加人 0.80 mol PC15,反应达平衡时 PC15还剩 0.60 mol ,其分解率 al等于_________________;若反应温度由 Tl升高到T2,平衡时 PC15的分解率为a2,a2_________ al(填“大于”、“小于”或“等于”) ;
(3)工业上制备 PC15通常分两步进行,先将 P 和 C12反应生成中间产物 PC13,然后降温,再和Cl2反应生成 PCl5。原因是___________________________________
______________________________________________________;
(4)P 和 C12分两步反应生成 1 mol PC15的△H3==__________________,一步反应生成 1 molPC15的△H4____________△H3(填“大于”、“小于”或“等于”)。
(5)PC15与足量水充分反应,最终生成两种酸,其化学方程式是
______________________________________________________________________。
(1)2P(s) + 3Cl2(g)=2PCl3(g);△H =-612kJ/mol
(2)PCl5(g)=PCl3(g) + Cl2(g);△H="+93kJ/mol " 25% 大于
(3) 两步反应都是放热反应,降温有利于提高产率,防止产物分解
(4) -399kJ/mol 等于
(5)PCl5 + 4H2O=H3PO4 + 5HCl
解析

 活力课时同步练习册系列答案
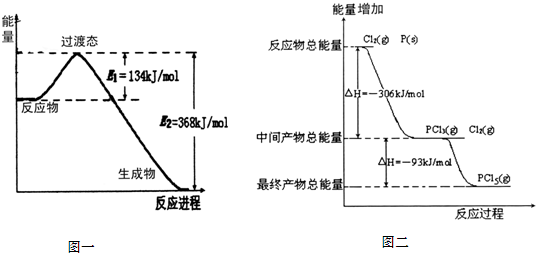
活力课时同步练习册系列答案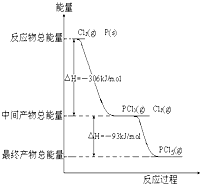 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图判断,下列叙述正确的是( )
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图判断,下列叙述正确的是( )| A、P和Cl2分两步反应生成1molPCl5的△H3=399 kJ?mol-1 | ||
| B、P和Cl2一步反应生成1molPCl5的△H4<△H3 | ||
C、P和Cl2反应生成PCl3的热化学方程式为:P(s)+
| ||
| D、PCl5分解成PCl3和Cl2的热化学方程式为:PCl5(g)=PCl3(g)+Cl2(g)△H=93kJ?mol-1 |

 红磷P(s)和Cl2(g)之间的反应为①P(s)+
红磷P(s)和Cl2(g)之间的反应为①P(s)+