题目内容
【题目】I.将少量饱和氯化铁溶液滴入沸水中,继续煮沸,可制得Fe(OH)3胶体,反应的方程式为: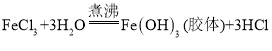 。
。
①当溶液呈________时,停止加热,即制得Fe(OH)3胶体。
②氢氧化铁胶体粒子直径大小的范围是____________________。
③下列叙述错误的是________。(单选)
A. 雾属于胶体,能产生丁达尔效应
B. “PM 2.5”悬浮在空气中形成胶体,危害人体健康 (“PM 2.5”指大气中直径小于或等于2.5微米的细小颗粒物,也可称为可吸入肺颗粒物)
C. 明矾、硫酸铁可以净水,净水原理和胶体有关
D. 胶体在一定条件下能稳定存在,属于介稳体系
Ⅱ.(1)下列4组物质均有一种物质的类别与其它3种不同
A. CaO、Na2O、CO2、CuO B. H2、C、P、Cu
C. O2、Fe、Cu、Zn D. HCl、H2O、H2SO4、HNO3
以上四组物质中与别不同的物质依次是(填化学式):
A________________;B________________;C________________;D________________。
(2)请对以下过程形成的分散系进行分类
①花生油加入到水中后充分搅拌; ②向蒸馏水中加入硝酸钾至恰好饱和;
③将饱和氯化铁溶液逐滴加入沸水中,继续加热,直至出现红褐色;
④澄清石灰水中通入少量的CO2; ⑤水和酒精的混合物;
属于浊液的是:________(填序号,下同);属于溶液的是:________。
(3)下列物质:①HCl ②蔗糖 ③NaOH ④KCl ⑤SO2 ⑥Fe ⑦碳酸钠溶液
属于电解质的是:___________(填序号),属于非电解质的是:___________(填序号),能导电的是:_____________________(填序号)。
【答案】红褐色 1~100 nm B CO2 Cu O2 H2O ①④ ②⑤ ①③④ ②⑤ ⑥⑦
【解析】
I.①制备氢氧化铁胶体,可将饱和氯化铁滴加到沸水中,并加热至溶液呈红褐色;
②胶体分散质粒子的直径在1nm~100nm之间;
③A.雾分散质粒子直径在1nm~100nm之间;
B.胶体的微粒直径在1-100nm之间;
C.明矾净水是水解生成氢氧化铝胶体净水;硫酸铁是水解生成氢氧化铁胶体净水;
D.胶体是介稳分散系。
Ⅱ.(1)根据物质的组成和性质进行分类;
(2)分散系可以根据分散质微粒直径的大小,分为浊液、胶体、溶液
(3)在水溶液或者熔融状态下,能导电的化合物为电解质;在水溶液或者熔融状态下,不能导电的化合物为非电解质;只要有自由移动的带电微粒就可以导电。
I. ①实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热;
②胶体分散质粒子的直径在1nm~100nm之间;
③A.雾分散质粒子直径在1nm~100nm之间,属于胶体,能产生丁达尔效应,故不选A;
B.“ “PM2.5”指大气中直径小于或等于2.5微米的细小颗粒物,直径大于100nm,在空气中形不成胶体,故选B;
C.明矾净水是水解生成氢氧化铝胶体净水;硫酸铁是水解生成氢氧化铁胶体净水;
,故不选C;
D.胶体在一定条件下能稳定存在,属于介稳体系,故不选D;
答案:B
Ⅱ.(1)A. CaO、Na2O、CuO为金属氧化物,CO2为非金属氧化物;
B.H2、C、P为非金属单质,Cu为金属单质;
C.Fe、Cu、Zn为金属单质,O2为非金属单质;
D.HCl、H2SO4、HNO3为酸,H2O不属于酸;
(2)①花生油加入到水中后充分搅拌,花生油难溶于水,形成乳浊液;
②向蒸馏水中加入硝酸钾至恰好饱和,形成溶液;
③将饱和氯化铁溶液逐滴加入沸水中,继续加热,直至出现红褐色,生成氢氧化铁胶体;
④澄清石灰水中通入少量的CO2,生成碳酸钙沉淀和水,属于悬浊液;
⑤水和酒精互溶,构成溶液;
(3)在水溶液或者熔融状态下,能导电的化合物为电解质,常见的电解质有酸、碱、盐、水,活泼金属的氧化物和过氧化物等,符合条件的有①③④;
在水溶液或者熔融状态下,不能导电的化合物为非电解质,符合条件的有②⑤;
只要有自由移动的带电微粒就可以导电,符合条件的有⑥⑦。