题目内容
能正确解释下列反应原理的离子方程式是( )
分析:A、碳酸根水解是分步进行的;
B、铝离子水解反应是可逆的;
C、离子反应要遵循电荷守恒;
D、碳酸氢钠可以和盐酸反应生成水以及氯化钠、二氧化碳.
B、铝离子水解反应是可逆的;
C、离子反应要遵循电荷守恒;
D、碳酸氢钠可以和盐酸反应生成水以及氯化钠、二氧化碳.
解答:解:A、碳酸钠溶液因为碳酸根离子水解而呈碱性,但是碳酸根水解是分步进行的,故A错误;
B、铝离子水解反应是可逆的,Al3++3H2O?Al(OH)3+3H+,故B错误;
C、离子反应要遵循电荷守恒,用三氯化铁溶液腐蚀印刷电路板上的铜:2Fe3++Cu═2Fe2++Cu2+,故C错误;
D、碳酸氢钠可以和盐酸反应生成水以及氯化钠、二氧化碳,实质是:HCO-3+H+═CO2↑+H2O,故D正确.
故选D.
B、铝离子水解反应是可逆的,Al3++3H2O?Al(OH)3+3H+,故B错误;
C、离子反应要遵循电荷守恒,用三氯化铁溶液腐蚀印刷电路板上的铜:2Fe3++Cu═2Fe2++Cu2+,故C错误;
D、碳酸氢钠可以和盐酸反应生成水以及氯化钠、二氧化碳,实质是:HCO-3+H+═CO2↑+H2O,故D正确.
故选D.
点评:本题考查学生水解方程式以及离子方程式书写方面知识,注意水解反应及水解程度,难度不大.

练习册系列答案
相关题目
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一.对下列事实解释正确的是( )
|
下列说法正确的是( )
| A、将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中必有铁 | ||
| B、饱和FeCl3溶液在20℃时呈现棕黄色,100℃呈现红褐色,不能用平衡移动原理来解释 | ||
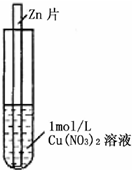
C、在
| ||
| D、在原电池装置中,电子从负极流出,沿导线流入正极,经溶液或盐桥回到负极 |
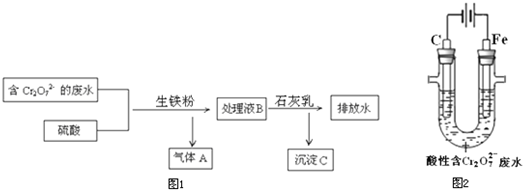
 (2011?上饶二模)如图,将一锌片放入1mol?L-1蓝色Cu(NO3)2溶液中,观察到下列实验现象:①反应初期锌片上有大量气泡冒出,同时液面的上一层Cu(NO3)2溶液开始呈现绿色,并且逐渐向液面下的深处扩散,试管底部有红色固体出现.②与锌片接触的溶液温度明显升高,反应越来越剧烈,并在红色固体上方开始出现一层蓝色沉淀,并逐渐增多.③反应后期溶液逐渐变为无色,试管底部又有部分白色沉淀物.
(2011?上饶二模)如图,将一锌片放入1mol?L-1蓝色Cu(NO3)2溶液中,观察到下列实验现象:①反应初期锌片上有大量气泡冒出,同时液面的上一层Cu(NO3)2溶液开始呈现绿色,并且逐渐向液面下的深处扩散,试管底部有红色固体出现.②与锌片接触的溶液温度明显升高,反应越来越剧烈,并在红色固体上方开始出现一层蓝色沉淀,并逐渐增多.③反应后期溶液逐渐变为无色,试管底部又有部分白色沉淀物.