题目内容
臭氧可用于净化空气、饮用水的消毒、处理工业废物和作氧化剂.
(1)臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:6Ag(s)+O3(g)=3Ag2O(s) ΔH=-235.8kJ/mol.已知2Ag2O(s)=4Ag(s)+O2(g) ΔH=+62.2kJ/mol,则常温下反应: 2O3(g)=3O2(g)的ΔH= .
(2)科学家P.Tatapudi等人首先使用在酸性条件下电解水的方法制得臭氧。臭氧在阳极周围的水中产生,电极反应式为3H2O-6e-=O3↑+6H+,阴极附近溶解在水中的氧气生成过氧化氢,其电极反应式为 。
(3)O3在碱性条件下可将Na2SO4氧化成Na2S2O8。写出该反应的化学方程式为:


(4)所得的Na2S2O8溶液可降解有机污染物4-CP。原因是Na2S2O8溶液在一定条件下可产生强氧化性自由基(SO4-·)。通过测定4-CP降解率可判断Na2S2O8溶液产生SO4-·的量。某研究小组设计实验探究了溶液酸碱性、Fe2+的浓度对产生SO4-·的影响。
①溶液酸碱性的影响:其他条件相同,将4-CP加入到不同pH的Na2S2O8溶液中,结果如图a所示。由此可知:溶液酸性增强, (填 “有利于”或“不利于”)Na2S2O8产生SO4-·。
②Fe2+浓度的影响:相同条件下,将不同浓度的FeSO4溶液分别加入c(4-CP)=1.56×10-4 mol·L-1、c(Na2S2O8)=3.12×10-3 mol·L-1的混合溶液中。反应240 min后测得实验结果如图b所示。已知 S2O82- + Fe2+= SO4-·+ SO42- + Fe3+。则由图示可知下列说法正确的是:_________________(填序号)
③当c(Fe2+)=3.2 ×10-3 mol·L-1时,4-CP降解的平均反应速率的计算表达式为 。
(1)臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:6Ag(s)+O3(g)=3Ag2O(s) ΔH=-235.8kJ/mol.已知2Ag2O(s)=4Ag(s)+O2(g) ΔH=+62.2kJ/mol,则常温下反应: 2O3(g)=3O2(g)的ΔH= .
(2)科学家P.Tatapudi等人首先使用在酸性条件下电解水的方法制得臭氧。臭氧在阳极周围的水中产生,电极反应式为3H2O-6e-=O3↑+6H+,阴极附近溶解在水中的氧气生成过氧化氢,其电极反应式为 。
(3)O3在碱性条件下可将Na2SO4氧化成Na2S2O8。写出该反应的化学方程式为:


(4)所得的Na2S2O8溶液可降解有机污染物4-CP。原因是Na2S2O8溶液在一定条件下可产生强氧化性自由基(SO4-·)。通过测定4-CP降解率可判断Na2S2O8溶液产生SO4-·的量。某研究小组设计实验探究了溶液酸碱性、Fe2+的浓度对产生SO4-·的影响。
①溶液酸碱性的影响:其他条件相同,将4-CP加入到不同pH的Na2S2O8溶液中,结果如图a所示。由此可知:溶液酸性增强, (填 “有利于”或“不利于”)Na2S2O8产生SO4-·。
②Fe2+浓度的影响:相同条件下,将不同浓度的FeSO4溶液分别加入c(4-CP)=1.56×10-4 mol·L-1、c(Na2S2O8)=3.12×10-3 mol·L-1的混合溶液中。反应240 min后测得实验结果如图b所示。已知 S2O82- + Fe2+= SO4-·+ SO42- + Fe3+。则由图示可知下列说法正确的是:_________________(填序号)
| A.反应开始一段时间内, 4-CP降解率随Fe2+浓度的增大而增大,其原因是Fe2+能使Na2S2O8产生更多的SO4-·。 |
| B.Fe2+是4-CP降解反应的催化剂 |
| C.当c(Fe2+)过大时,4-CP降解率反而下降,原因可能是Fe2+会与SO4—.发生反应,消耗部分SO4—.。 |
| D.4-CP降解率反而下降,原因可能是生成的Fe3+水解使溶液的酸性增强,不利于降解反应的进行。 |
(1)-285.0KJ.mol-1(3分)
(2)3O2 + 6H+ +6e- = 3H2O2(或O2 +2H+ +2e- = H2O2) (3分)
(3)2Na2SO4 + O3 + H2O = Na2S2O8 + 2NaOH + O2 (3分)
(4) ①有利于 (2分)
②AC(2分)
③
 (3分)
(3分)
(2)3O2 + 6H+ +6e- = 3H2O2(或O2 +2H+ +2e- = H2O2) (3分)
(3)2Na2SO4 + O3 + H2O = Na2S2O8 + 2NaOH + O2 (3分)
(4) ①有利于 (2分)
②AC(2分)
③

 (3分)
(3分) 试题分析:(1)根据盖斯定律,所求方程式可由3×②-1×①而得,所以ΔH="3×(+62.2kJ/mol)" -2×(-235.8kJ/mol)= -285.0KJ.mol-1 。
(2)由于电解水法制臭氧实质是电解溶解有氧气的水溶液3O2 + 3H2O = O3↑+3H2O2 ,虽然酸性条件下,但算不参加反应,所以电解过程中阳极发生的氧化反应为H2O失电子变成臭氧,而不能是OH-,阴极发生的还原反应为O2得电子变成H2O2,所以阴极电极反应式为:O2 +2H+ +2e- = H2O2 ,若要阴阳极得失电子统一,也可写成3O2 + 6H+ +6e- = 3H2O2 。
(3)O3在碱性条件下将Na2SO4氧化成Na2S2O8的反应是一个氧化还原反应,要注意的是O3的性质和O2相比,臭氧有较强的氧化性,而且不稳定,容易变成为O2,所以在该反应中,O3中O原子不是全部做氧化剂,部分化合价不变;而Na2SO4 中S由+6价→+7价,所以找出相应的氧化剂、还原剂、氧化产物和还原产物后,用缺项配平书写化学方程式得:2Na2SO4 + O3 + H2O = Na2S2O8 + 2NaOH + O2 。
(4)①图a中明显可以看出,随着横坐标pH的增大,4-CP降解率逐渐减小,而起到降解作用的是具有强氧化性的自由基(SO4-·),所以讲解率降低说明强氧化自由基减少,所以酸性增强才有利于Na2S2O8产生SO4-·。
②根据图b可以看出,开始的一段时间内随着横坐标Fe2+浓度增大,4-CP降解率在增大,所以说明在这段时间内,Fe2+能使Na2S2O8产生更多的SO4-·,A正确。强氧化性自由基是通过S2O82- + Fe2+= SO4-·+ SO42- + Fe3+反应产生的,所以Fe2+ 不是讲解反应的催化剂,B错误;因为自由基SO4-·有强氧化性,所以若Fe2+ 浓度过大,则来不及反应的Fe2+ 会被生成的自由基氧化,导致自由基减少,降解率下降,C正确,D错误;故选AC。
③当c(Fe2+)=3.2 ×10-3 mol·L-1时,从图像b中可以找到此时的降解率52.4%,而初始浓度为c(4-CP)=1.56×10-4 mol·L-1 ,所以在240min内的反应速率v=△C/△t=

 。
。
练习册系列答案
相关题目

 mol
mol mol
mol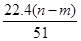 L
L +
+ 的酸性溶液,使溶液中的Fe2+恰好全部氧化,并使
的酸性溶液,使溶液中的Fe2+恰好全部氧化,并使 是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生如下反应:
是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生如下反应: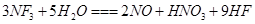 。下列有关该反应的说法正确的是
。下列有关该反应的说法正确的是 是还原剂
是还原剂 非极性分子,在潮湿空气中泄漏会看到红棕色气体
非极性分子,在潮湿空气中泄漏会看到红棕色气体 个电子
个电子