题目内容
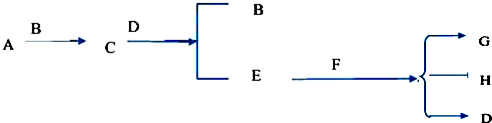
19.化合物A和D都是石油裂解气的成分,是衡量一个国家化工水平的重要标志的物质的同系物,可利用如下反应合成化合物H:
已知:
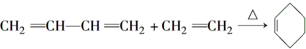
请回答下列问题:
(1)反应①~⑥中属于加成反应的是①⑤(填序号,下同),属于氧化反应的是③④.
(2)写出反应④的化学方程式:
 .
.(3)写出G的结构简式:
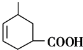 ,G中官能团的名称为羧基和碳碳双键.
,G中官能团的名称为羧基和碳碳双键.(4)写出反应⑥的化学方程式:
 .
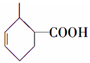
.(5)化合物C与化合物F反应还可以生成化合物G的同分异构体,其结构简式为
 .
.(6)下列有关化合物H的说法正确的是AD(填字母).
A.化合物H在一定温度下能与NaOH溶液发生水解反应
B.化合物H的分子式为C10H13O2
C.1mol化合物H与H2发生加成反应,消耗3mol H2
D.化合物H能使溴水褪色.
分析 根据题中各物质转化关系,G在浓硫酸作用下发生酯化反应得H,由H的结构可知G为 ,化合物A和D都是石油裂解气的成分,结合其分子式可知其为不饱和烃,根据A和C的分子式要知,A与溴发生加成反应生成B,B在氢所化钠的醇溶液中发生消去反应生成C,比较D和E的分子式可知,D发生氧化反应生成E,E能与氢氧化铜反应,则E为醛,F为羧酸,结合G的结构可知C和F发生题中信息中的加成反应生成G,根据G可推知C为CH2=CHCH=CHCH3,F为CH2=CHCOOH,所以B为CH3CHBrCHBrCH2CH3,A为CH3CH=CHCH2CH3,E为CH2═CHCHO,D为CH2═CHCH3,据此答题.
,化合物A和D都是石油裂解气的成分,结合其分子式可知其为不饱和烃,根据A和C的分子式要知,A与溴发生加成反应生成B,B在氢所化钠的醇溶液中发生消去反应生成C,比较D和E的分子式可知,D发生氧化反应生成E,E能与氢氧化铜反应,则E为醛,F为羧酸,结合G的结构可知C和F发生题中信息中的加成反应生成G,根据G可推知C为CH2=CHCH=CHCH3,F为CH2=CHCOOH,所以B为CH3CHBrCHBrCH2CH3,A为CH3CH=CHCH2CH3,E为CH2═CHCHO,D为CH2═CHCH3,据此答题.
解答 解:根据题中各物质转化关系,G在浓硫酸作用下发生酯化反应得H,由H的结构可知G为 ,化合物A和D都是石油裂解气的成分,结合其分子式可知其为不饱和烃,根据A和C的分子式要知,A与溴发生加成反应生成B,B在氢所化钠的醇溶液中发生消去反应生成C,比较D和E的分子式可知,D发生氧化反应生成E,E能与氢氧化铜反应,则E为醛,F为羧酸,结合G的结构可知C和F发生题中信息中的加成反应生成G,根据G可推知C为CH2=CHCH=CHCH3,F为CH2=CHCOOH,所以B为CH3CHBrCHBrCH2CH3,A为CH3CH=CHCH2CH3,E为CH2═CHCHO,D为CH2═CHCH3,
,化合物A和D都是石油裂解气的成分,结合其分子式可知其为不饱和烃,根据A和C的分子式要知,A与溴发生加成反应生成B,B在氢所化钠的醇溶液中发生消去反应生成C,比较D和E的分子式可知,D发生氧化反应生成E,E能与氢氧化铜反应,则E为醛,F为羧酸,结合G的结构可知C和F发生题中信息中的加成反应生成G,根据G可推知C为CH2=CHCH=CHCH3,F为CH2=CHCOOH,所以B为CH3CHBrCHBrCH2CH3,A为CH3CH=CHCH2CH3,E为CH2═CHCHO,D为CH2═CHCH3,
(1)根据上面的分析可知,反应①~⑥中属于加成反应的是①⑤,属于氧化反应的是③④,
故答案为:①⑤;③④;
(2)反应④的化学方程式为CH2═CHCHO+2Cu(OH)2 $\stackrel{△}{→}$CH2═CHCOOH+Cu2O↓+2H2O,
故答案为:CH2═CHCHO+2Cu(OH)2 $\stackrel{△}{→}$CH2═CHCOOH+Cu2O↓+2H2O;
(3)根据上面的分析可知,G为 ,含有的官能团为羧基和碳碳双键,
,含有的官能团为羧基和碳碳双键,
故答案为: ;羧基和碳碳双键;
;羧基和碳碳双键;
(4)反应⑥的化学方程式为 ,
,
故答案为: ;
;
(5)C为CH2=CHCH=CHCH3,是不对称烯,所以化合物C与化合物F反应还可以生成化合物G的同分异构体,其结构简式为 ,
,
故答案为: .
.
(6)根据化合物H的结构简式可知,
A.化合物H中有酯基,在一定温度下能与NaOH溶液发生水解反应,故A正确;
B.化合物H的分子式为C10H16O2,故B错误;
C.1mol化合物H与H2发生加成反应,消耗1mol H2,故C错误;
D.化合物H中有碳碳双键,能使溴水褪色,故D正确,
故选AD.
点评 本题考查有机物的结构与性质、化学方程式的书写、有机物的推断等,题目难度不大,注意常见有机物的性质即可解答该题.

| A. | 玻璃杯 | B. | 羊毛毯 | C. | 塑料啤酒箱 | D. | 铝合金窗 |
| 化学反应 | 平衡常数 | 温度℃ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | ||
(2)某温度下反应①中H2的平衡转化率(α)与体系总压强(p)的关系如图1所示.则平衡状态由A变到B时,平衡常数KA=KB(填“>”、“<”或“=”).据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1•K2(用K1、K2表示),反应③为放热反应(填“吸热”或“放热”).
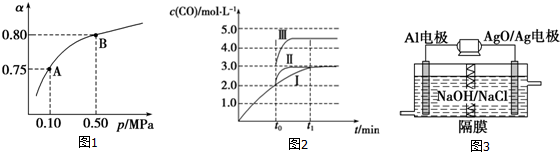
(3)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ.
当曲线Ⅰ变为曲线Ⅱ时,改变的条件是加入催化剂.
当曲线Ⅰ变为曲线Ⅲ时,改变的条件是将容器的体积快速压缩至2L.
(4)甲醇燃料电池有着广泛的用途,同时Al-AgO电池是应用广泛的鱼雷电池,其原理如图3所示.则该电池的负极反应式是Al-3e-+4OH-=AlO2-+2H2O.
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸.通常状况下,将a mol•L-1的醋酸与b mol•L-1 Ba(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为$\frac{2b}{a-2b}×1{0}^{-7}$L/mol.
| A. | H+、Fe2+、Al3+、NO3- | B. | Na+、Al3+、Cl-、Fe2+ | ||
| C. | OH-、Al3+、Cl-、NO3- | D. | OH-、Ba2+、Cl-、NO3- |
| A. | pH=0的溶液呈中性 | |
| B. | 溶液pH相差3,则c(H+)相差30倍 | |
| C. | pH=5的HCl加水稀释1000倍后,溶液pH=8 | |
| D. | pH=5的CH3COOH溶液酸性比pH=6的HCl溶液的酸性强 |