题目内容
A和B反应生成C,假定反应由A、B开始,它们的起始浓度均为1mol/L.反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L.则2min内反应的平均速率VA=
0.1mol?L-1?min-1
0.1mol?L-1?min-1
,VB=0.2mol?L-1?min-1
0.2mol?L-1?min-1
,VC=0.3mol?L-1?min-1
0.3mol?L-1?min-1
.该反应的化学反应方程式为A+2B=3C
A+2B=3C
.分析:根据v=
计算出2min内用物质A、B、C表示的平均反应速率,再利用速率之比等于化学计量数之比确定系数,书写化学反应方程式.
| △c |
| △t |
解答:解:v(A)=
=0.1 mol?L-1?min-1,
v(B)=
=0.2 mol?L-1?min-1,
v(C)=
=0.3 mol?L-1?min-1,
所以,v(A):v(B):v(C)=0.1 mol?L-1?min-1:0.2 mol?L-1?min-1:0.3 mol?L-1?min-1=1:2:3,
化学计量数之比等于速率之比,反应方程式为A+2B=3C.
故答案为:V(A)=0.1 mol?L-1?min-1 V(B)=0.2 mol?L-1?min-1 V(C)=0.3 mol?L-1?min-1
A+2B=3C
| 1mol/L-0.8mol/L |
| 2min |
v(B)=
| 1mol/L-0.6mol/L |
| 2min |
v(C)=
| 0.6mol/L |
| 2min |
所以,v(A):v(B):v(C)=0.1 mol?L-1?min-1:0.2 mol?L-1?min-1:0.3 mol?L-1?min-1=1:2:3,
化学计量数之比等于速率之比,反应方程式为A+2B=3C.
故答案为:V(A)=0.1 mol?L-1?min-1 V(B)=0.2 mol?L-1?min-1 V(C)=0.3 mol?L-1?min-1
A+2B=3C
点评:考查化学反应速率的有关计算等,难度不大,注意基础知识的积累掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
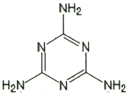

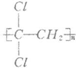 )具有超强阻隔性能,可作为保鲜食品的包装材料.它是由
)具有超强阻隔性能,可作为保鲜食品的包装材料.它是由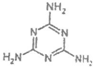

 ______.
______.