题目内容
【题目】过氧化钠与铝粉混合物共18.3g,加入1L水,充分反应后混合物完全溶解,并收集到5.6L气体(标准状况下)
(1)计算生成的气体的总质量____;
(2)计算反应后溶液中各溶质的物质的量浓度(该溶液体积不变)____。
【答案】3.5g 0.3 mol/L 0.1 mol/L
【解析】
发生反应有:2Na2O2![]() 2H2O=4NaOH
2H2O=4NaOH![]() O2↑,2Al
O2↑,2Al![]() 2NaOH
2NaOH![]() 2H2O=2NaAlO2
2H2O=2NaAlO2![]() 3H2↑。
3H2↑。
(1)生成的气体为氧气与氢气,过氧化钠与Al都反应,令过氧化钠与Al的物质的量分别为x mol、y mol,根据二者质量之和及生成气体的体积之和列方程,据此计算解答;
(2)结合方程式计算判断NaOH是否完全反应、生成偏铝酸钠的物质的量,确定NaOH物质的量,再根据![]() 计算。
计算。
(1)设过氧化钠与Al的物质的量分别为x mol、y mol,过氧化钠与Al都反应,则:![]() ,
,
xmol![]()
![]()
![]() ,
,
ymolymol ymol![]() 所以
所以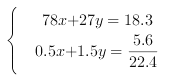 ,计算得出:
,计算得出:![]() ,
,![]() ,即混合物中由过氧化钠0.2mol,铝0.1mpl,由上述反应可知,生成O2为0.5x=0.1mol,m(O2)=0.1mol
,即混合物中由过氧化钠0.2mol,铝0.1mpl,由上述反应可知,生成O2为0.5x=0.1mol,m(O2)=0.1mol![]() 32g/mol=3.2g,生成H2为1.5y=0.15mol,m(H2)=0.15mol
32g/mol=3.2g,生成H2为1.5y=0.15mol,m(H2)=0.15mol![]() 2g/mol=0.3g,所以共生成气体3.5g;
2g/mol=0.3g,所以共生成气体3.5g;
本题答案为:3.5g。
(2)由方程式可以知道,过氧化钠反应生成氢氧化钠为0.4mol,Al反应消耗的NaOH为![]() 、生成的偏铝酸钠为
、生成的偏铝酸钠为![]() ,故溶液中氢氧化钠为0.4mol-0.1mol=0.3mol,溶液中氢氧化钠的物质的量浓度c(NaOH)=0.3mol/1L=0.3mol/L,偏铝酸钠的物质的量浓度c(NaAlO2)=0.1mol/1L=0.1mol/L,;
,故溶液中氢氧化钠为0.4mol-0.1mol=0.3mol,溶液中氢氧化钠的物质的量浓度c(NaOH)=0.3mol/1L=0.3mol/L,偏铝酸钠的物质的量浓度c(NaAlO2)=0.1mol/1L=0.1mol/L,;
本题答案为:0.3mol/L,0.1mol/L。

练习册系列答案
相关题目