题目内容
【题目】物质的量浓度相同的下列溶液中,含微粒种类最多的是( )
A.CaCl2B.CH3COONaC.NH4ClD.Na2S
【答案】D
【解析】
A. CaCl2溶液中,含有Ca2+、Cl-、H+、OH-、H2O,共5种微粒;
B. CH3COONa溶液中,含有CH3COO-、Na+、H+、OH-、H2O、CH3COOH,共6种微粒;
C. NH4Cl溶液中,含有NH4+、Cl-、H+、OH-、NH3·H2O、H2O,共6种微粒;
D. Na2S溶液中,含有Na+、S2-、HS-、H+、OH-、H2S、H2O,共7种微粒。
综合以上分析,Na2S溶液中所含微粒的种类最多。故选D。

【题目】对甲基苯胺可用对硝基甲苯在酸性条件下用铁粉还原制得:

主要反应物和产物的物理性质见下表:
化合物 | 物质状态 | 溶解性 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) |
对硝基甲苯 | 浅黄色晶体 | 不溶于水,溶于乙醇、苯 | 51.4 | 237.7 | 1.286 |
对甲基苯胺 | 白色片状晶体 | 微溶于水,易溶于乙醇、苯 | 43~45 | 200~202 | 1.046 |
对甲基苯胺盐酸盐 | 白色晶体 | 易溶于水,不溶于乙醇、苯 | 243~245 | —— | —— |
苯 | 无色液体 | 不溶于水,溶于乙醇 | 5.5 | 80.1 | 0.874 |
实验流程如下:

请回答下列问题:
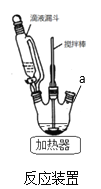
(1)反应装置如图,a处缺少一装置_____________(填仪器名称)
(2)步骤②中加苯的作用是_____________,步骤②中用5%碳酸钠溶液调pH=7~8的原因_________
(3)步骤③得到的固体物质为_________
(4)步骤④中加入盐酸的作用是_____________
(5)步骤⑤中通过加入氢氧化钠溶液使对甲基苯胺结晶析出的原理为_____________
(6
A. 蒸馏水 B.乙醇 C.NaOH溶液 D.HCl溶液