��Ŀ����
����Ŀ��2019����ʷ�������֯��ȫ��̼�ƻ���12��4�շ������棺�о���ʾ��ȫ�������̼�ŷ��������� ����CO2���ۺ������ǽ�������������Ч;����
��1��һ��;���ǽ�CO2ת�����л���ʵ��̼ѭ�����磺
![]()
![]()
![]() ��H3=____
��H3=____
��2��CO2���黯��Ӧ���ɷ�����ѧ��Paul Sabatier����ģ���ˣ��÷�Ӧ�ֽ�Sabatier��Ӧ��CO2���⻯ �Ƽ�����о��������£�
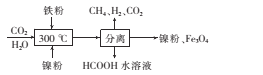
�����������У�����H2��Ӧ�Ļ�ѧ����ʽΪ____
��HCOOH��CO2ת��ΪCH4���м��壺CO2![]() HCOOH
HCOOH![]() CH4����������������10������IJ���Ѹ�ټ��٣���������������ʱ��CO2�����⻯�Ƽ����������Ӧ�з�Ӧ�������ӽϴ��һ����_____����I������������
CH4����������������10������IJ���Ѹ�ټ��٣���������������ʱ��CO2�����⻯�Ƽ����������Ӧ�з�Ӧ�������ӽϴ��һ����_____����I������������
��3��CO2��������������ɵ�̼������Ҫ������������Ӧ��
��ӦI: ![]()
��Ӧ����![]()
��1 L�����ܱ������г���1 mol CO2��4 mol H2�����ƽ��ʱ�й����ʵ����ʵ������¶ȱ仯��ͼ��ʾ��T1��ʱ��CO2��ת����Ϊ____��T1��ʱ����ӦI��ƽ�ⳣ��K= ___��
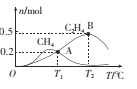
��4����֪CO2������ϳ��Ҵ��ķ�Ӧԭ��Ϊ![]() ��m������ʼʱ��Ͷ�ϱȣ���
��m������ʼʱ��Ͷ�ϱȣ���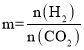
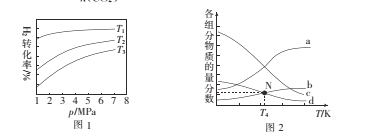
��ͼ1��Ͷ�ϱ���ͬ���¶�T3>T2>T1�����H ______������>������<����0��
��m=3ʱ���÷�Ӧ�ﵽƽ��״̬��p���ܣ�=20a MPa����ѹ�����¸����ʵ����ʵ����������¶ȵĹ�ϵ��ͼ2��������b����������Ϊ ___���ѧʽ����T4�¶�ʱ����Ӧ�ﵽƽ��ʱ����d�ķ�ѹp��d��=______
���𰸡�+1366.8kJmol-1 3Fe+4H2O![]() Fe3O4+4H2 �� 60% 0.045 �� CO2 2.5aMPa
Fe3O4+4H2 �� 60% 0.045 �� CO2 2.5aMPa
��������
(1)��֪��Ӧ��C2H4(g)+H2O(l)�TC2H5OH (l)��H1=-44.2kJmol-1
��2CO2(g)+2H2O(l)�TC2H4(g)+3O2(g)��H2=+1411.0 kJmol-1
��ϸ�˹���ɣ���Ӧ��+�ڽ�ϵã�2CO2(g)+3H2O(l)�TC2H5OH(l)+3O2(g)��H3=��H1+��H2=-44.2kJmol-1+1411.0 kJmol-1=+1366.8kJmol-1��
(2)�ٸ�������ͼ��֪��Ӧ��Ϊ��Fe��H2O��������Ϊ��H2��Fe3O4����ѧ����ʽΪ��3Fe+4H2O![]() Fe3O4+4H2��
Fe3O4+4H2��
�ڵ�������������10������IJ�����Ѹ�ټ��٣�˵��������������ʴ������������ʣ����˵����Ӧ��������Ҫ�ȷ�Ӧ�����������ӵÿ죻
(3)T1��ʱ��ϵ��n(CH4)=0.2mol������ݷ�Ӧ����CO2(g)+4H2(g)CH4(g)+2H2O(g)��֪�÷�Ӧ���ĵ�n(CO2)=0.2mol�����ĵ�n(H2)=0.8mol�����ɵ�n(H2O)=0.4mol����ϵ��n(C2H4)=0.2mol������ݷ�Ӧ����2CO2(g)+6H2(g)C2H4(g)+4H2O(g)��֪�÷�Ӧ���ĵ�n(CO2)=0.4mol�����ĵ�n(H2)=1.2mol�����ɵ�n(H2O)=0.8mol��������n(CO2)=0.2mol+0.4mol=0.6mol��������(CO2)=![]() ��100%=60%��
��100%=60%��
���������Ϊ1L������ƽ��ʱ��c(CO2)=![]() =0.4mol/L��c(H2)=
=0.4mol/L��c(H2)=![]() =2mol/L��c(CH4)=
=2mol/L��c(CH4)=![]() =0.2mol/L��c(H2O)=
=0.2mol/L��c(H2O)=![]() =1.2mol/L��ƽ�ⳣ��K=
=1.2mol/L��ƽ�ⳣ��K=![]() =0.045��
=0.045��
(4)�ٸ���ͼʾ����ͬѹǿ��Ͷ�ϱȵ������£��¶�Խ�ߣ�H2ת����Խ�ͣ�˵������ӦΪ���ȷ�Ӧ����H��0��
���¶����ߣ���Ӧ������У����Բ�������ʵ��������ٵģ���Ӧ������ʵ���������ͼ��֪������a����������ΪH2��b��ʾCO2��cΪH2O��dΪC2H5OH��
m=3ʱ����n(CO2)=3mol��n(H2)=9mol��������ʽ���£�
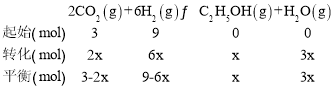
����ͼʾ��n(CO2)=n(C2H5OH)����3-2x=x�����x=1mol��C2H5OH���������=![]() =
=![]() =12.5%��p(C2H5OH)=20aMPa��12.5%=2.5aMPa��
=12.5%��p(C2H5OH)=20aMPa��12.5%=2.5aMPa��

 ������ϵ�д�
������ϵ�д� �±�Сѧ��Ԫ�Բ���ϵ�д�
�±�Сѧ��Ԫ�Բ���ϵ�д�����Ŀ��2019��ŵ������ѧ����������ӵ�صķ����ߣ�LiFePO4������ӵ�ص��������ϡ��ú�﮷�������Ҫ����Ԫ�صĺ�����Li 8.50%��Ni 6.55%��Mg 13.24%���Ʊ�Li2C2O4���������Ʊ�LiFePO4���ֹ���������ͼ�������̿������ˮ������Ⱦ����
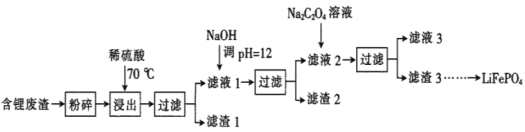
��֪����Һ1����Һ2�в������ӵ�Ũ�ȣ�g��L-1����
Li+ | Ni2+ | Mg2+ | |
��Һ1 | 22.72 | 20.68 | 60.18 |
��Һ2 | 21.94 | 7.7��10-3 | 0.78��10-3 |
I.�Ʊ�Li2C2O4
(1)����2����Ҫ�ɷ���__���ѧʽ����
(2)Na2C2O4��Һ�и����ӵ�Ũ���ɴ�С˳��Ϊ__��
(3)д������Na2C2O4��Һʱ������Ӧ�����ӷ���ʽ��__��
��.�Ʊ�LiFePO4
(4)����ؼ�Li2C2O4��FePO4���ڸ����·�Ӧ����LiFePO4��һ���������壬�÷�Ӧ�Ļ�ѧ����ʽ��___��
(5)LiFePO4��Ҫ�ڸ����³��ͺ������Ϊ�缫�����³���ʱҪ��������ʯī����ʯī��������__����дһ�㣩��
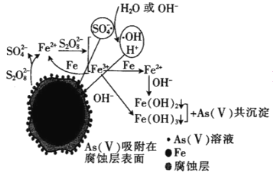
(6)�ҹ���ѧ���о��������������ƣ�Na2S2O8��ȥ����ˮ�е�As(��)�������ģ����ͼ�������������������Ʒ�Ӧ�����ӷ���ʽ��__���ڸ�ģ���еõ������鹲�����ᆳ���գ���Ԫ�ػ��ϼ۱仯����õ�һ�ִ��Ի������ѧʽΪFe7As2O14���������ж��������������ĸ�����Ϊ__��