题目内容
 实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量.测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时,Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出.
实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量.测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时,Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出.(1)写出Na2CO3完全转化为NaHCO3的离子方程式
(2)某天然碱的化学式为xNa2CO3?NaHCO3?2H2O,为了测定其组成,取0.3320g样品于锥形瓶中,加适量蒸馏水使之溶解,加入几滴酚酞,用0.1000mol?L-1的盐酸滴定至溶液由红色变无色,消耗盐酸20.00mL;再向已变无色的溶液中加入几滴甲基橙,继续用该盐酸滴定至溶液由黄色变橙色,又消耗盐酸30.00mL.
①实验时用到的玻璃仪器有烧杯、胶头滴管、锥形瓶、
②该天然碱化学式中x=
(3)某学习小组在实验室中制备Na2CO3,假设产品中含有少量NaCl、NaHCO3杂质,设计实验方案进行检验,完成下表.
限选试剂:0.1000mol?L-1盐酸、稀硝酸、AgNO3溶液、酚酞、甲基橙、蒸馏水.
| 实验步骤 | 结果分析 |
| 步骤①:取少量样品于试管中,加入适量蒸馏水使之溶解, |
有白色沉淀生成,说明产品中含有NaC1 |
| 步骤②:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000mol?L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积Vl; |
品中含有NaHCO3 |
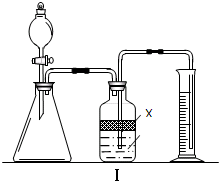
①广口瓶中的试剂X可以选用
A.苯B.酒精C.植物油D.CCl4
②广口瓶的液体没有装满(上方留有少量空间),实验测得二氧化碳的体积将
(2))①根据操作步骤判断所使用的玻璃仪器;
②两次消耗的盐酸分别是20ml和30ml,因此根据方程式可知,样品中碳酸钠和碳酸氢钠的物质的量之比是2:1,以此确定x;
(3)检验氯离子一般用硝酸酸化的硝酸银溶液,现象是生成氯化银白色沉淀;根据反应的方程式可知,如果含有碳酸氢钠,则第二次消耗的盐酸体积大于第一次消耗的盐酸体积;
(4)①X的作用是液封,密度比水的大,还要不溶于水;
②广口瓶的液体没有装满不影响测定结果.
故答案为:CO32-+H+=HCO3-;
(2))①溶解样品还需要玻璃棒玻璃棒;滴定是还需要酸式滴定管盛放盐酸,
故答案为:玻璃棒、酸式滴定管;
②两次消耗的盐酸分别是20ml和30ml,方程式分别是CO32-+H+=HCO3-、HCO3-+H+=CO2↑+H2O,因此根据方程式可知,样品中碳酸钠和碳酸氢钠的物质的量之比是2:1,所以x=2,故答案为:2;
(3)检验氯离子一般用硝酸酸化的硝酸银溶液,现象是生成氯化银白色沉淀;根据反应的方程式可知,如果含有碳酸氢钠,则第二次消耗的盐酸体积大于第一次消耗的盐酸体积,即V2>V1,故答案为:①滴加足量的稀硝酸酸化,再加几滴硝酸银溶液;②再向一变无色的溶液中滴加几滴甲基橙,继续用该盐酸溶液滴定至溶液由黄色变成橙色;V2>V1;
(4)①广口瓶中的试剂X作用是封住二氧化碳气体,密度必须比水的密度小,还不能溶于水,选项中满足的有A、C,故选AC;
②广口瓶的液体没有装满,不会影响测定的结果,故答案为:不变.

(16分)实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量。测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出。(化学式量:Na2CO3-106,NaHCO3-84)
(1)分别写出上述转化反应的离子方程式:
________ _ ___、_______ ______。
(2)某天然碱的化学式为xNa2CO3·NaHCO3·2H2O,为了测定其组成,取0.3320 g样品于锥形瓶中,加适量蒸馏水使之溶解,加入几滴酚酞,用0.1000 mol·L-1的盐酸滴定至溶液由红色变无色,消耗盐酸20.00mL;再向已变无色的溶液中加入几滴甲基橙,继续用该盐酸滴定至溶液由黄色变橙色,又消耗盐酸30.00mL。
①实验时用到的玻璃仪器有烧杯、胶头滴管、锥形瓶、____________。
②该天然碱化学式中x=_____ ____。
(3)某学习小组在实验室中制备Na2CO3,假设产品中含有少量NaCl、NaHCO3杂质,设计实验方案进行检验,完成下表。
限选试剂:0.1000 mol·L-1盐酸、稀硝酸、AgNO3溶液、酚酞、甲基橙、蒸馏水
| 实验步骤 | 结果分析 |
| 步骤1:取少量样品于试管中,加入适量蒸馏水使之溶解,_____________________。 | 有白色沉淀生成,说明产品中含有NaCl。 |
| 步骤2:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000 mol·L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积V1。 _____________________,记录消耗盐酸的体积V2。 | ______ ______, 说明产品中含有NaHCO3。 |
(16分)实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量。测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出。(化学式量:Na2CO3-106,NaHCO3-84)
(1)分别写出上述转化反应的离子方程式:
________ _ ___、_______ ______。
(2)某天然碱的化学式为xNa2CO3·NaHCO3·2H2O,为了测定其组成,取0.3320 g样品于锥形瓶中,加适量蒸馏水使之溶解,加入几滴酚酞,用0.1000 mol·L-1的盐酸滴定至溶液由红色变无色,消耗盐酸20.00mL;再向已变无色的溶液中加入几滴甲基橙,继续用该盐酸滴定至溶液由黄色变橙色,又消耗盐酸30.00mL。
① 实验时用到的玻璃仪器有烧杯、胶头滴管、锥形瓶、____________。
② 该天然碱化学式中x=_____ ____。
(3)某学习小组在实验室中制备Na2CO3,假设产品中含有少量NaCl、NaHCO3杂质,设计实验方案进行检验,完成下表。
限选试剂:0.1000 mol·L-1盐酸、稀硝酸、AgNO3溶液、酚酞、甲基橙、蒸馏水
|
实验步骤 |
结果分析 |
|
步骤1:取少量样品于试管中,加入适量蒸馏水使之溶解,_____________________。 |
有白色沉淀生成,说明产品中含有NaCl。 |
|
步骤2:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000 mol·L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积V1。
_____________________,记录消耗盐酸的体积V2。 |
______ ______, 说明产品中含有NaHCO3。 |
 实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量.测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时,Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出.
实验室中可用盐酸滴定的方法测定Na2CO3或NaHCO3的含量.测定Na2CO3时,若用酚酞作指示剂,逐滴加入盐酸至溶液由红色变无色时,Na2CO3完全转化为NaHCO3;测定NaHCO3时,若用甲基橙作指示剂,逐滴加入盐酸至溶液由黄色变橙色时NaHCO3完全转化为CO2逸出.
(1)写出Na2CO3完全转化为NaHCO3的离子方程式______.
(2)某天然碱的化学式为xNa2CO3?NaHCO3?2H2O,为了测定其组成,取0.3320g样品于锥形瓶中,加适量蒸馏水使之溶解,加入几滴酚酞,用0.1000mol?L-1的盐酸滴定至溶液由红色变无色,消耗盐酸20.00mL;再向已变无色的溶液中加入几滴甲基橙,继续用该盐酸滴定至溶液由黄色变橙色,又消耗盐酸30.00mL.
①实验时用到的玻璃仪器有烧杯、胶头滴管、锥形瓶、______.
②该天然碱化学式中x=______.
(3)某学习小组在实验室中制备Na2CO3,假设产品中含有少量NaCl、NaHCO3杂质,设计实验方案进行检验,完成下表.
限选试剂:0.1000mol?L-1盐酸、稀硝酸、AgNO3溶液、酚酞、甲基橙、蒸馏水.
| 实验步骤 | 结果分析 |
| 步骤①:取少量样品于试管中,加入适量蒸馏水使之溶解, ______ | 有白色沉淀生成,说明产品中含有NaC1 |
| 步骤②:另取少量样品于锥形瓶中,加入适量蒸馏水使之溶解,加入几滴酚酞,用0.1000mol?L-1盐酸滴定至溶液由红色变无色,记录消耗盐酸的体积Vl;______,记录消耗盐酸的体积V2 | ______,说明产 品中含有NaHCO3 |
①广口瓶中的试剂X可以选用______.
A.苯B.酒精C.植物油D.CCl4
②广口瓶的液体没有装满(上方留有少量空间),实验测得二氧化碳的体积将______(填“偏高”、“偏低”或“不变”).