题目内容
某学生设计了如下图所示的方法对A盐溶液进行鉴定:
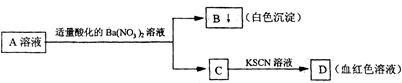
由此分析,下列结论中不正确的是 ( )

由此分析,下列结论中不正确的是 ( )
| A.A中一定有Fe3+ | B.C中一定有Fe3+ |
| C.A可能为Fe2(SO4)3 | D.B一定为BaSO4 |
A
试题分析:A中不一定有铁离子,因为如果A只含有亚铁离子也由此现象,故A错误,为本题的答案;B正确,C中一定含有铁离子;C正确,A可以为Fe2(SO4)3,D也正确,因为硫酸钡为白色沉淀,不溶于硝酸。
点评:本题考查了离子检验的知识,该知识点是高考常常考查的,本题要理解A中不一定含有铁离子,若要检验则直接在A中滴加KSCN,看是否出现血红色,若是,则说明一定含有铁离子,若不是则说明含有的是亚铁离子,本题难度中等。

练习册系列答案
相关题目