题目内容
12.下列反应的离子方程式书写正确的是.( )| A. | 向Ba(OH)2溶液中加入NaHSO4溶液至刚好沉淀完全:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | Cu与浓H2SO4 共热:Cu+4H++SO42-$\frac{{\underline{△}}}{\;}$ZCu2++SO2↑+2H2O | |
| C. | 向FeSO4溶液中滴加H2O2溶液:Fe2++H2O2+2H+═Fe3++2H2O | |
| D. | 将SO2通入Ca(ClO)2溶液:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO |
分析 A.沉淀刚好完全时,氢氧化钡与硫酸氢钠的物质的量之比为1:1;
B.浓硫酸在离子方程式中不能拆开,应该两边分子式;
C.离子方程式两边正电荷不相等,违反了电荷守恒;
D.次氯酸能够将亚硫酸钙氧化成硫酸钙.
解答 解:A.向Ba(OH)2溶液中加入NaHSO4溶液至刚好沉淀完全,此时氢氧化钡与硫酸氢钠的物质的量相等,反应的离子方程式为:Ba2++OH-+H++SO42-═BaSO4↓+H2O,故A正确;
B.铜与浓硫酸的反应中,浓硫酸不能拆开,正确的离子方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;△\;}}{\;}$Cu2++SO2↑+2H2O+SO42-,故B错误;
C.向FeSO4溶液中滴加H2O2溶液,二者发生氧化还原反应,正确的离子方程式为:2Fe2++H2O2+2H+═2Fe3++2H2O,故C错误;
D.次氯酸具有强氧化性,能够将亚硫酸钙氧化成硫酸钙,当二氧化硫过量时,反应的离子方程式为:Ca2++3ClO-+H2O+SO2═CaSO4↓+2HClO+Cl-,故D错误;
故选A.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式正误判断常用方法,如:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
2.对于可逆H2(g)+I2(g)$\stackrel{△}{?}$2HI(g),下列情况一定能说明反应已达到平衡状态的是( )
| A. | 气体总压强不再随时间而改变时 | |
| B. | 气体的总质量不再改变时 | |
| C. | 混合气体中各组成成分的含量不再改变时 | |
| D. | 单位时间内每消耗1 mol I2,同时有2 mol HI生成时 |
3.对达到平衡状态的可逆反应:A+B?C+D,在t1时增大压强,则正、逆反应速率变化如图所示(v表示反应速率,t代表时间),下列有关A、B、C、D的状态叙述正确的是( )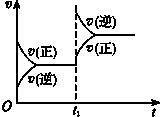

| A. | A、B都是气体,C、D都不是气体 | B. | A、B都是气体,C、D有一种是气体 | ||
| C. | C、D都是气体,A、B都是气体 | D. | C、D都是气体,A、B有一种是气体 |
20.下列反应中,生成物的总能量大于反应物的总能量的是( )
| A. | 氢气在氧气中燃烧 | B. | 焦炭在高温下与水蒸气反应 | ||
| C. | 铝与三氧化二铁高温反应 | D. | 铁丝在氧气中燃烧 |
17.下列说正确的是( )
| A. | 存在自由移动的离子是电解质溶液导电的原因 | |
| B. | 由于电流的作用,酸、碱、盐溶于水发生电离 | |
| C. | 电解质在熔融状态下都能导电 | |
| D. | 在水溶液中电离出氢离子的化合物属于酸 |
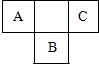 A、B、C为短周期元素,在周期表中所处位置如图所示.
A、B、C为短周期元素,在周期表中所处位置如图所示.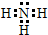 ;
;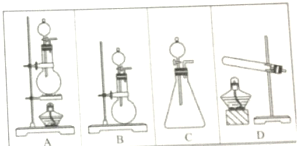 实验室里现有下列装置和试剂制取少量氯化氢气体时选用:①浓硫酸②浓盐酸③食盐固体④硫酸氢钠固体⑤二氧化锰固体请用实验装置编号回答:
实验室里现有下列装置和试剂制取少量氯化氢气体时选用:①浓硫酸②浓盐酸③食盐固体④硫酸氢钠固体⑤二氧化锰固体请用实验装置编号回答: