题目内容
【题目】常温下,下列有关0.lmol·L-1的NH4Cl溶液的说法正确的是
A. pH相同的盐酸与氯化铵溶液中,水的电离程度相同
B. 加入少量Mg(OH)2固体,c(NH4+)减小
C. 溶液加水稀释时, 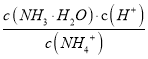 逐渐增大
逐渐增大
D. 加入等体积0. 05 mol L-1的NaOH溶液时: c(Na+) =c(Cl-) >c(NH4+)>c(OH-)>c( H+)
【答案】B
【解析】A、盐酸抑制水的电离,氯化铵水解促进水的电离,pH值相同的盐酸和氯化铵溶液中水的电离程度前者小于后者,选项A错误;B、加入少量Mg(OH)2固体,消耗氯化铵水解生成的氢离子,促进铵根离子的水解,使c(NH4+)减小,选项B正确;C、溶液加水稀释时, 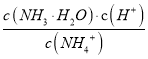 =
=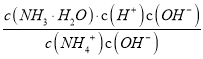 =
=![]() ,温度不变,
,温度不变, 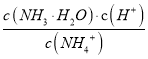 不变,选项C错误;D、加入等体积0. 05 mol L-1的NaOH溶液时,可看成是溶质为NH4Cl和NH3H2O按1:1的溶液,且溶液呈碱性,则有c(Cl-) >c(NH4+)> c(Na+)>c(OH-)>c( H+),选项D错误。答案选B。
不变,选项C错误;D、加入等体积0. 05 mol L-1的NaOH溶液时,可看成是溶质为NH4Cl和NH3H2O按1:1的溶液,且溶液呈碱性,则有c(Cl-) >c(NH4+)> c(Na+)>c(OH-)>c( H+),选项D错误。答案选B。

练习册系列答案
相关题目
【题目】一定温度下,10 mL 0.40 mol/L H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)( )
A. 0~6 min的平均反应速率: v(H2O2)≈3.3×10-2mol·L-1·min-1
B. 0~6 min的平均反应速率: v(H2O2)<3.3×10-2mol·L-1·min-1
C. 反应至6 min时,c(H2O2)=0.30 mol/L
D. 反应至6 min时,H2O2分解了50%