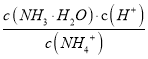��Ŀ����
����Ŀ������Ԫ������Sn����̼Ԫ��λ��ͬһ���壬��Ҫ���ϼ�Ϊ+2��+4��ijͬѧͨ�����з����ⶨ��������Ʒ�Ĵ��ȣ����ٶ����ʲ��μӷ�Ӧ��
��1�����������������У���Ӧ�Ļ�ѧ����ʽΪ��______________________��
��2�����������FeCl3��Һ����Ӧ�Ļ�ѧ����ʽΪ��______________________��
��3������֪Ũ�ȵ�K2Cr2O7������Һ�ζ����ɵ�Fe2������Ӧ�����ӷ���ʽΪ��______________
��4�����н�������Ʒ1.142g��������������Ӧ����ȥ0.100mol/L��K2Cr2O7��Һ16.00ml. ��������������������_____________________��
��5�����裨4�������ȡ��16.00ml��K2Cr2O7��Һ��Ӧ��____________�����������ƣ�����ͬѧ������0.100mol/L ��K2Cr2O7��Һ�������У����������趼��ȷ��������ʱ���ӿ̶�����������Һ��Ũ��____________����ƫ�ߣ�ƫ�ͣ�����Ӱ�죩��
���𰸡� Sn+2HCl=SnCl2+H2�� SnCl2+2 FeCl3= SnCl4+2 FeCl2 6Fe2++CrO72+14H+=6 Fe3++2Cr3++7 H2O 50.0�� ��ʽ�ζ��ܣ�����Һ�ܣ� ƫ��
����������1�����������������У��������ᷴӦ�����Ȼ�������������Ӧ�Ļ�ѧ����ʽΪ��Sn+2HCl=SnCl2+H2������2�����������FeCl3��Һ���Ȼ������Ȼ�������������ԭ��Ӧ�������Ȼ������Ȼ���������Ӧ�Ļ�ѧ����ʽΪ��SnCl2+2 FeCl3= SnCl4+2 FeCl2����3������֪Ũ�ȵ�K2Cr2O7������Һ�ζ����ɵ�Fe2����CrO72-����ԭΪCr3+��Fe2��������ΪFe3+����Ӧ�����ӷ���ʽΪ��6Fe2++CrO72-+14H+=6 Fe3++2Cr3++7 H2O����4����������������������Ϊx���������淴Ӧ�ɵù�ϵʽ��
3Sn~~~~~~~~~~~~ K2Cr2O7
3��119 1
1.142x 0.100mol/L��0.016L
x=![]() ��100%=50%��
��100%=50%��
��5�����裨4�������ȡ��16.00ml��K2Cr2O7��Һ��Ӧ����ʽ�ζ��ܻ���Һ�ܣ�������ʱ��������ƿ�̶��������ˮ�����ƫ�٣�������Һ��Ũ��ƫ�ߡ�

 ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д� ���������ν�ϵ�д�
���������ν�ϵ�д�����Ŀ���±��Ǽ������᳣���µĵ���ƽ�ⳣ����
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8��10-5 | K1=4.3��10-7 K2=5.6��10-11 | K1=9.1��10-8 K2=1.1��10-12 | K1=7.5��10-3 K2=6.2��10-8 K3=2.2��10-13 |
������˵���в���ȷ���ǣ�������
A. ̼�������ǿ��������
B. �����£���ˮϡ�ʹ��ᣬ![]() ����
����
C. ��Ԫ�����������Ҫ�ɵ�һ���������
D. ��������Һ�м�����NaOH��Һ�����볣������