题目内容
(8分)在0.1 mol/L氨水中,分别加入少量下列物质,溶液中的c(OH-)如何变化?(填“增大”、“减小”或“不变”)
⑴加少量HNO3溶液____________ ⑵加少量KOH溶液___________
⑶加少量(NH4)2SO4固体__________ (4)加大量水__________
⑴加少量HNO3溶液____________ ⑵加少量KOH溶液___________
⑶加少量(NH4)2SO4固体__________ (4)加大量水__________
(1)减小 (2)增大 (3)减小 (4)减小
考查外界条件对电离平衡的影响。一水合氨的电离方程式为NH3·H2O NH4++OH-,因此加少量HNO3溶液平衡向右移动,c(OH-)减小;加少量KOH溶液平衡向逆反应方向移动,但c(OH-)增大;加少量(NH4)2SO4固体平衡向逆反应方向移动,c(OH-)减小;加水有利于电离,但碱性会降低,即c(OH-)减小。
NH4++OH-,因此加少量HNO3溶液平衡向右移动,c(OH-)减小;加少量KOH溶液平衡向逆反应方向移动,但c(OH-)增大;加少量(NH4)2SO4固体平衡向逆反应方向移动,c(OH-)减小;加水有利于电离,但碱性会降低,即c(OH-)减小。
 NH4++OH-,因此加少量HNO3溶液平衡向右移动,c(OH-)减小;加少量KOH溶液平衡向逆反应方向移动,但c(OH-)增大;加少量(NH4)2SO4固体平衡向逆反应方向移动,c(OH-)减小;加水有利于电离,但碱性会降低,即c(OH-)减小。
NH4++OH-,因此加少量HNO3溶液平衡向右移动,c(OH-)减小;加少量KOH溶液平衡向逆反应方向移动,但c(OH-)增大;加少量(NH4)2SO4固体平衡向逆反应方向移动,c(OH-)减小;加水有利于电离,但碱性会降低,即c(OH-)减小。
练习册系列答案
相关题目
 2C在不同温度下经过一定时间,混合物中C的百分含量与温度关系如下图所示,那么:
2C在不同温度下经过一定时间,混合物中C的百分含量与温度关系如下图所示,那么: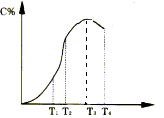 (1)反应在___________________温度下达到化学平衡;
(1)反应在___________________温度下达到化学平衡; 3Z(g)+2W(g),达到化学平衡时,测出的下列各生成物浓度的数据中肯定错误的是( )
3Z(g)+2W(g),达到化学平衡时,测出的下列各生成物浓度的数据中肯定错误的是( ) N2O4(g);△H<0,在测定NO2的相对分子质量时,下列条件较为适宜的是
N2O4(g);△H<0,在测定NO2的相对分子质量时,下列条件较为适宜的是 SO3(g)达到平衡,SO2的转化率前者大
SO3(g)达到平衡,SO2的转化率前者大 N2O4(g)达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡时,与第一次平衡时相比,NO2的体积分数增大
N2O4(g)达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡时,与第一次平衡时相比,NO2的体积分数增大 PH3(g) + HI(g) ① ;
PH3(g) + HI(g) ① ; 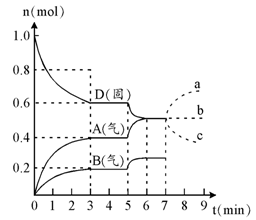
 B(?)+ 2C(?) △H>0,满足如图所示的关系,则下列说法中正确的是
B(?)+ 2C(?) △H>0,满足如图所示的关系,则下列说法中正确的是 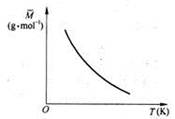
 CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下: