题目内容
【题目】由U形管、质量为m g的铁棒、质量为m g的碳棒和1 L 0.2 mol·L-1 CuCl2溶液组成的装置如图所示,下列说法正确的是
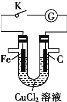
A.打开K,铁棒上有紫红色物质析出
B.闭合K,碳棒上有紫红色固体析出
C.闭合K,当电路中有0.3NA个电子通过时,理论上碳棒与铁棒的质量差为9.6 g
D.闭合K,铁棒表面发生的电极反应为Cu2++2e-=Cu
【答案】AB
【解析】
A. 打开K,Fe直接与CuCl2溶液反应生成Cu,所以铁棒上有紫红色物质析出,故A正确;
B. 闭合K,形成原电池,Fe作负极、碳棒作正极,溶液中的Cu2+在正极上得电子生成Cu,所以碳棒表面发生的电极反应为Cu2++2e-=Cu,碳棒上有紫红色固体析出,故B正确;
C. 闭合K,形成原电池,Fe作负极、碳棒作正极,负极反应为Fe-2e-=Fe2+,正极反应:Cu2++2e-=Cu,当电路中有0.3NA个(0.3mol)电子通过时,负极减少0.15 molFe(质量为8.4g),正极增加0.15mol Cu(质量为9.6g),所以理论上碳捧与铁棒的质量差为18g,故C错误;
D. 闭合K,形成原电池,Fe作负极、碳棒作正极,溶液中的Cu2+在正极上得电子生成Cu,所以碳棒表面发生的电极反应为Cu2++2e-=Cu,故D错误;
答案选AB。

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】实验室用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如图所示:

有关数据列表如下:
乙醇 | 1,2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -l30 | 9 | -116 |
回答下列问题:
(1)写出该实验过程中发生的所有主要反应的化学方程式____;
在此制各实验中,要尽可能迅速地把反应温度170℃左右,其最主要目的是___(填正确选项前的字母,下同)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入__,其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)将1,2二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___层,若产物中有少量未反应的Br2,最好用____洗涤除去。
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(4)若产物中有少量副产物乙醚。可用____的方法除去,加热方式为____。
(5)反应过程中应用___冷却装置D
A.冰水混合物 B.室温下的水 C.60℃ D.100℃
【题目】对羟基苯甲酸乙酯广泛用于食品、化妆品、医药等领域。某化学兴趣小组通过查阅文献,制备羟基苯甲酸乙酯。回答下列问题:
(一)对羟基苯甲酸乙酯的合成
实验原理: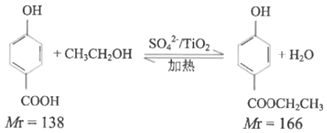
实验步骤:取0.4mol乙醇和催化剂置于干燥的仪器A中,0.1mol对羟基苯甲酸置于恒压滴液漏斗C中,实验装置如图所示(加热和夹持装置省略)。加热回流,充分反应。
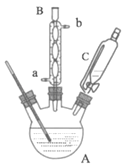
(1)仪器A的名称是_____。仪器B中冷凝水的流向为从_____(“a”或“b”)通入。
(2)某同学准备在仪器A和球形冷凝管之间加一个脱水装置,用化学平衡原理解释这样做的优点是_____。
(3)取催化剂2g,对羟基苯甲酸0.1mol,乙醇0.4mol,反应过程中酯的产率与反应时间的关系如下表所示:
反应时间/小时 | 1 | 3 | 4 | 5 | 6 |
酯的产率/% | 45.6 | 88 | 91.8 | 91.1 | 90.8 |
根据表中数据可知,最佳反应的时间应为_____;反应时间过长,产率有所下降的可能原因是_____。
(二)对羟基苯甲酸乙酯的精制
实验方法:①反应完毕后趁热滤出催化剂,滤液倒入冷水中,析出固体,过滤。
②固体先后用5%的Na2CO3溶液和水洗涤,干燥后得到粗产品。
③在装有冷凝管的圆底烧瓶中,按照一定比例加入粗品酯、乙醇、水和活性炭,加热回流0.5小时,趁热抽滤,滤液冷却,析出白色晶体,于80℃烘干。
(4)在②中用5%的Na2CO3溶液洗涤的目的是_____,能不能用NaOH溶液替代?_____(填“能”或“不能”)。
(5)在③趁热抽滤主要除去的杂质为_____,“趁热”的目的是_____。
(6)该小组同学按(3)中数据投料,最后得到对羟基苯甲酸乙酯14.9g,则该实验的产率为_____%。
【题目】相同温度下,根据三种酸的电离平衡常数,下列判断正确的是![]()
酸 | HX | HY | HZ |
|
|
|
|
A.三种酸的强弱关系: ![]()
B.反应 ![]() 能够发生
能够发生
C.相同温度下,![]() 的NaX、NaY、NaZ溶液,NaZ溶液pH最大
的NaX、NaY、NaZ溶液,NaZ溶液pH最大
D.相同温度下,![]() 溶液的电离常数大于
溶液的电离常数大于![]()