题目内容
12.等质量的O2和O3,它们的物质的量之比为3:2,所含分子数之比为3:2,所含原子数之比为1:1,相同状况下的体积之比为3:2.分析 根据n=$\frac{m}{M}$可知,等质量的O2和O3,它们的物质的量之比与摩尔质量成反比;根据N=nNA可知,分子数目之比等于物质的量之比;O2和O3均由O原子构成,二质量相等,含有氧原子数目相等;相同条件下,体积之比等于物质的量之比;
解答 解:根据n=$\frac{m}{M}$可知,等质量的O2和O3,它们的物质的量之比=48g/mol:32g/mol=3:2;
根据N=nNA可知,O2和O3所含分子数目之比=O2和O3物质的量之比=3:2;
O2和O3均由O原子构成,二质量相等,含有氧原子数目相等,即含有氧原子数目之比为1:1;
相同条件下,O2和O3体积之比=O2和O3的物质的量之比=3:2,
故答案为:3:2;3:2;1:1;3:2.
点评 本题考查物质的量有关计算,注意对公式的理解与灵活应用,侧重对基础知识的巩固,题目难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
2.下列有关叙述错误的是( )
| A. | 化学反应均伴随着能量的变化 | |
| B. | 需要加热才能发生的反应不一定是吸热反应 | |
| C. | 物质的化学能可以在一定条件下转化为热能、电能为人类利用 | |
| D. | 吸热反应中由于反应物总能量小于生成物总能量,因而没有利用价值 |
20.体积为1L的干燥容器中充入一定量HCl气体后,测得容器中气体对氧气的相对密度为1.082.则容器中HCl气体的质量分数约为( )
| A. | 75% | B. | 25% | C. | 79.1% | D. | 78.1% |
7.通过书写化学方程式举出反例,证明下列说法不正确.
| 氧化反应一定属于化合反应 | CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O |
| 生成盐和水的反应一定是中和反应 | Ca(OH)2+CO2═CaCO3↓+H2O |
| 只有在加热或高温条件下才能冶炼出金属 | Fe+CuSO4═FeSO4+Cu |
17.下图分别表示四种操作,其中有两处错误的是( )
| A. | 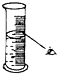 读数 | B. | 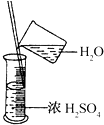 稀释 | C. | 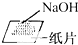 称量 | D. | 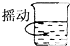 溶解 |
4.目前科学家提出了一种最经济最理想的获得氢能源的循环体系(如图).下列说法错误的是( )


| A. | 在此循环中发生了反应:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | |
| B. | 燃料电池是将化学能转化为电能的装置 | |
| C. | 该氢能源的循环体系能够实现太阳能转化为电能 | |
| D. | 目前化学家急需解决的问题是寻找合适的光照条件下分解水的催化剂 |
1.下列属于天然高分子化合物的组合是( )
| A. | 天然橡胶、淀粉 | B. | 油脂、蛋白质 | C. | 塑料、纤维素 | D. | 蔗糖、淀粉 |
2.下列说法不正确的是 ( )
| A. | 具有较高能量的反应物分子称为活化分子 | |
| B. | 升高温度增大了活化分子百分数 | |
| C. | 化剂能够改变化学反应途径 | |
| D. | 增大压强能提高活化分子的浓度 |