题目内容
(1)CH3+、-CH3(甲基)、CH3-都是重要的有机反应中间体,有关它们的说法正确的是
A、它们均由甲烷去掉一个氢原子所得
B、它们互为等电子体,碳原子均采取sp2杂化
C、CH3-与NH3、H2O+互为等电子体,几何构型均为三角锥形
D、CH3+中的碳原子采取sp2杂化,所有原子均共面
E、两个-CH3(甲基)或一个CH3+'和一个CH3-结合均可得到CH3CH3
(2)锌是一种重要的金属,锌及其化合物有着广泛的应用.
①锌在元素周期表中的位置是: .
②葡萄糖酸锌〔CH2OH( CHOH) 4 COO]2Zn是目前市场上流行的补锌剂.写出Zn2+基态电子排布式 ,葡萄糖分子[CH2OH(CHOH)4CHO]中碳原子杂化方式有
③Zn2+能与NH3形成配离子[Zn(NH3)4]2+.配位体NH3分子属于 (填“极性分子”或“非极性分子”);在〔Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在图1中表示出〔Zn(NH3)4]2+中Zn2+与N之间的化学键.

④图2示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的Zn与X的原子个数之比为 ;
⑤在④的晶胞(图2)中,如果只考查X的排列方式,则X的堆积方式属于金属晶体堆积方式中的_ 堆积;设该晶胞中Zn的半径为r1 cm,其相对原子质量为M1,X的半径为r2cm,其相对原子质量为M2,则该晶体的密度为_ g/cm3(写出 含有字母的表达式)
A、它们均由甲烷去掉一个氢原子所得
B、它们互为等电子体,碳原子均采取sp2杂化
C、CH3-与NH3、H2O+互为等电子体,几何构型均为三角锥形
D、CH3+中的碳原子采取sp2杂化,所有原子均共面
E、两个-CH3(甲基)或一个CH3+'和一个CH3-结合均可得到CH3CH3
(2)锌是一种重要的金属,锌及其化合物有着广泛的应用.
①锌在元素周期表中的位置是:
②葡萄糖酸锌〔CH2OH( CHOH) 4 COO]2Zn是目前市场上流行的补锌剂.写出Zn2+基态电子排布式
③Zn2+能与NH3形成配离子[Zn(NH3)4]2+.配位体NH3分子属于

④图2示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的Zn与X的原子个数之比为
⑤在④的晶胞(图2)中,如果只考查X的排列方式,则X的堆积方式属于金属晶体堆积方式中的_
考点:晶胞的计算,判断简单分子或离子的构型,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:(1)A.甲烷去掉一个氢原子不能得到CH3+、CH3-;
B.CH3+、CH3-、CH3-分别具有6个、7个和8个价电子,不是等电子体;
C.CH3-与NH3、H3O+均具有10个电子,互为等电子体,所以空间构型相同;
D.CH3+中的碳原子采取sp2杂化;
E.两个CH3-或一个CH3+和CH3-结合都能得到CH3CH3.
(2)①Zn的原子序数是30,在第四周期,ⅡB 族,ds 区;
②葡萄糖里有两种碳原子,葡萄糖是无羟基醛,所以,一种是以sp3杂化(接羟基的碳),一种是以sp2杂化(醛基里的碳);
③同种元素之间形成非极性共价键,不同元素之间形成极性共价键,分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,这样的分子为极性分子,以极性键结合的双原子一定为极性分子,以极性键结合的多原子分子如结构对称,正负电荷的重心重合,电荷分布均匀,则为非极性分子;[Zn(NH3)4]2+中Zn2+与N之间的化学键是配位键;
④利用均摊法可计算出晶胞中原子个数,据此得出原子个数比;
⑤根据晶胞结构图可知,X原子分布在晶胞立方体的顶点和面心上,是面心立方最密堆积,根据ρ=
,可算出密度.
B.CH3+、CH3-、CH3-分别具有6个、7个和8个价电子,不是等电子体;
C.CH3-与NH3、H3O+均具有10个电子,互为等电子体,所以空间构型相同;
D.CH3+中的碳原子采取sp2杂化;
E.两个CH3-或一个CH3+和CH3-结合都能得到CH3CH3.
(2)①Zn的原子序数是30,在第四周期,ⅡB 族,ds 区;
②葡萄糖里有两种碳原子,葡萄糖是无羟基醛,所以,一种是以sp3杂化(接羟基的碳),一种是以sp2杂化(醛基里的碳);
③同种元素之间形成非极性共价键,不同元素之间形成极性共价键,分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,这样的分子为极性分子,以极性键结合的双原子一定为极性分子,以极性键结合的多原子分子如结构对称,正负电荷的重心重合,电荷分布均匀,则为非极性分子;[Zn(NH3)4]2+中Zn2+与N之间的化学键是配位键;
④利用均摊法可计算出晶胞中原子个数,据此得出原子个数比;
⑤根据晶胞结构图可知,X原子分布在晶胞立方体的顶点和面心上,是面心立方最密堆积,根据ρ=
| m |
| V |
解答:
解:(1)A.甲烷分子变成CH3+、CH3-、CH3-时,失去的分别是氢负离子、氢离子和质子,空间构型也不再与原来的分子相同,故A错误;
B.CH3+、CH3-、CH3-分别具有6个、7个和8个价电子,不是等电子体,中心碳原子的价层电子对数不同,故空间构型不同,故B错误;
C.CH3-与NH3、H3O+均具有10个电子,互为等电子体,几何构型均为三角锥形,故C正确;
D.CH3+中的碳原子采取sp2杂化,所有原子均共面,故D正确;
E.两个CH3-或一个CH3+和CH3-结合可得到CH3CH3,故E正确.
故选CDE;
(2)①Zn的原子序数是30,其电子排布式为:1s22s22p63s23p63d104s2,由电子排布式可知该元素为第四周期,第ⅡB族,故答案为:第四周期第ⅡB族;
②Zn2+基态电子排布式为:1s22s22p63s23p63d10或[Ar]3d10,葡萄糖里有两种碳原子,葡萄糖是无羟基醛,所以,一种是以sp3杂化(接羟基的碳),一种是以sp2杂化(醛基里的碳),故答案为:1s22s22p63s23p63d10或[Ar]3d10;sp2、sp3;
③配位体NH3分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,是极性分子;[Zn(NH3)4]2+中Zn2+与N之间的化学键是配位键,
故答案为:极性分子;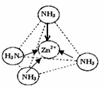 ;
;
④根据晶胞结构图可知,晶胞中锌的个数为4,X的个数为8×
+6×
=4,所以锌原子与X原子的个数比为1:1,故答案为:1:1;
⑤根据晶胞结构图可知,X原子分布在晶胞立方体的顶点和面心上,是面心立方最密堆积,在每个晶胞中含有4个锌原子和4个X原子,在晶胞结构中,晶胞的体对角线长度为4(r1+r2),所以晶胞的边长为
,根据ρ=
,可知密度为
g/cm3=
g/cm3,故答案为:面心立方最密;
.
B.CH3+、CH3-、CH3-分别具有6个、7个和8个价电子,不是等电子体,中心碳原子的价层电子对数不同,故空间构型不同,故B错误;
C.CH3-与NH3、H3O+均具有10个电子,互为等电子体,几何构型均为三角锥形,故C正确;
D.CH3+中的碳原子采取sp2杂化,所有原子均共面,故D正确;
E.两个CH3-或一个CH3+和CH3-结合可得到CH3CH3,故E正确.
故选CDE;
(2)①Zn的原子序数是30,其电子排布式为:1s22s22p63s23p63d104s2,由电子排布式可知该元素为第四周期,第ⅡB族,故答案为:第四周期第ⅡB族;
②Zn2+基态电子排布式为:1s22s22p63s23p63d10或[Ar]3d10,葡萄糖里有两种碳原子,葡萄糖是无羟基醛,所以,一种是以sp3杂化(接羟基的碳),一种是以sp2杂化(醛基里的碳),故答案为:1s22s22p63s23p63d10或[Ar]3d10;sp2、sp3;
③配位体NH3分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,是极性分子;[Zn(NH3)4]2+中Zn2+与N之间的化学键是配位键,
故答案为:极性分子;
 ;
;④根据晶胞结构图可知,晶胞中锌的个数为4,X的个数为8×
| 1 |
| 8 |
| 1 |
| 2 |
⑤根据晶胞结构图可知,X原子分布在晶胞立方体的顶点和面心上,是面心立方最密堆积,在每个晶胞中含有4个锌原子和4个X原子,在晶胞结构中,晶胞的体对角线长度为4(r1+r2),所以晶胞的边长为
| 4(r1+r2) | ||
|
| m |
| V |
| ||||
[
|
3
| ||
| 16NA(r1+r2)3 |
3
| ||
| 16NA(r1+r2)3 |
点评:本题考查判断简单分子或离子的构型、极性分子、晶胞的计算、原子轨道杂化方式及杂化类型判断、晶体类型的判断等,难度较大,掌握晶胞的计算是解题的关键

练习册系列答案
相关题目
1L 0.2mol/L的KI溶液中,含溶质KI的物质的量是( )
| A、0.2 mol |
| B、0.5 mol |
| C、2 mol |
| D、5 mol |
金刚石与石墨是碳的两种同素异形体,在100kPa时,1mol石墨转化为金刚石要吸收1.895kJ的热量,下列说法正确的是( )
| A、金刚石比石墨稳定 |
| B、1mol石墨比1mol金刚石的总能量低 |
| C、1mol石墨比1mol金刚石的总能量高 |
| D、石墨比金刚石稳定 |
下列实验操作正确的是( )
| A、给容量瓶检漏时,向容量瓶中注入适量水,左手托住瓶底右食指顶住瓶塞,倒置数次,观察是否漏水 |
| B、具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量 |
| C、配制一定物质的量浓度的溶液时,蒸馏水洗净后容量瓶未干燥,不影响测定结果 |
| D、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
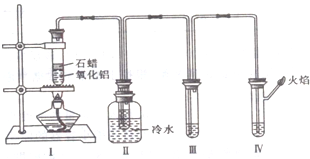
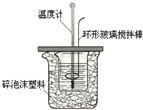 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题: