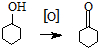题目内容
11.A~E是几种烃分子的球棍模型,据此回答下列问题:
(1)含碳量最高的烃是
 (填结构简式);
(填结构简式);(2)能够发生加成反应的烃有CD(填结构简式);
(3)互为同系物的烃有CH4、CH3CH3、CH3CH2CH3(填结构简式);
(4)写出C与溴水反应的化学方程式CH2═CH2+Br2→CH2BrCH2Br.
(5)描述D与溴水混合并充分振荡、静置后的现象分层,上层呈现橙红色,下层无色.
分析 有结构模型可知A为甲烷,B为乙烷,C为乙烯,D为苯,E为丙烷,根据物质的组成、结构和性质解答该题.
(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最大即为含碳量最高的.
(2)含有碳碳双键或三键或苯环的烃能发生加成反应.
(3)根据同系物的概念:结构相似,分子组成相差整数倍个CH2的有机物来回答;
(4)乙烯中含有双键,可以和溴水之间发生加成反应;
(5)苯和溴水混合,苯在溴水中的溶解度大于水中的溶解度.
解答 解:有结构模型可知A为甲烷,B为乙烷,C为乙烯,D为苯,E为丙烷,
(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最大即为含碳量最高的,所以含碳量最大的是苯,
故答案为: ;
;
(2)含有碳碳双键或三键或苯环的烃能发生加成反应,所以乙烯、乙炔、能发生加成反应,故答案为:CD;
(3)A为甲烷,B为乙烷,E为丙烷结构相似,分子组成相差整数倍个CH2,互为同系物,故答案为:CH4、CH3CH3、CH3CH2CH3;
(4)乙烯中含有双键,可以和溴水之间发生加成反应,与溴水反应的化学方程式为:CH2═CH2+Br2→CH2BrCH2Br,
故答案为:CH2═CH2+Br2→CH2BrCH2Br;
(5)苯在溴水中的溶解度大于水中的溶解度,苯和溴水混合并充分振荡、静置后的现象:分层,上层呈现橙红色,下层无色,故答案为:分层,上层呈现橙红色,下层无色.
点评 本题考查有机物的结构和性质,题目难度不大,注意把握有机物的结构特点,根据结构模型判断有机物的种类,为解答该题的关键.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
1.一定温度下,在密闭容器中充入4mol X,当反应4X(g)?3Y(g)+Z(g)达到平衡状态时,有30%的X发生分解,则达到平衡状态时混合气体的总物质的量是( )
| A. | 4 mol | B. | 3.4 mol | C. | 2.8 mol | D. | 1.2 mol |
19.如表实验现象和结论相符的是( )
| 操作及现象 | 结论 | |
| A | 某溶液中加入氯化钡溶液,产生白色沉淀,再加入稀硝酸沉淀不溶解 | 溶液中一定含有SO42- |
| B | 某溶液中加入硝酸银溶液,产生白色沉淀 | 溶液中一定含有Cl- |
| C | 用洁净铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色 | 溶液中有Na+,无K+ |
| D | 向某溶液中先加几滴KSCN溶液,无明显现象,再滴氯水,溶液变红 | 溶液中一定含有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
6.已知X、Y元素同周期.且电负性X>Y,下列说法一定错误的是( )
| A. | 第一电离能Y小于X | |
| B. | 最高价含氧酸的酸性:X对应的酸的酸性强于Y | |
| C. | 气态氢化物的稳定性:HmY强于HnX | |
| D. | X和Y形成化合物时,X显负价,Y显正价 |
16.下列关于钠的叙述中,正确的是( )
| A. | 钠是淡黄色固体 | |
| B. | 钠的密度:小于煤油大于水 | |
| C. | 钠在化学反应中只能做还原剂 | |
| D. | 钠与硫酸铜溶液反应有红色的铜生成 |
3.下列反应属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )
| A. | 2Na+2H2O=2NaOH+H2↑ | B. | Cl2+H2O═HCl+HClO | ||
| C. | 2H2O═2H2↑+O2↑ | D. | Na2O+H2O═2NaOH |
1.装置如图,通电后,发现Cu极附近溶液蓝色加深.下列说法正确的是( )


| A. | A极为负极,Cu为阳极 | |
| B. | 左烧杯溶液和右烧杯溶液的pH都变小 | |
| C. | 左烧杯Pt极和右烧杯Fe极的电解产物物质的量之比为1:1 | |
| D. | 左烧杯溶液浓度变大,右烧杯溶液浓度不变 |
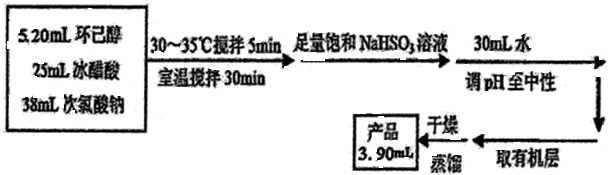
 环己酮是重要化工原料,是制造尼龙、己内酰胺和己二酸的主要中间体.某化学兴趣小组尝试用次氯酸钠制备环己酮.方程式为:
环己酮是重要化工原料,是制造尼龙、己内酰胺和己二酸的主要中间体.某化学兴趣小组尝试用次氯酸钠制备环己酮.方程式为: