题目内容
【题目】金属(M)-空气电池具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:2M+O2+2H2O=2M(OH)2。
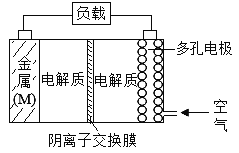
(已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能)下列说法正确的是
A.电解质中的阴离子向多孔电极移动
B.比较Mg、Al、Zn三种金属-空气电池,Mg-空气电池的理论比能量最高
C.空气电池放电过程的负极反应式2M-4e-+4OH-=2M(OH)2
D.当外电路中转移4mol电子时,多孔电极需要通入空气22.4L(标准状况)
【答案】C
【解析】
A.原电池中阴离子应该向负极移动;
B.电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,即单位质量的电极材料失去电子的物质的量越多,则得到的电能越多;
C.负极M失电子和OH反应生成M(OH)2;
D.由正极电极反应式O2+2H2O+4e=4OH有O2~4OH~4e,当外电路中转移4mol电子时,消耗氧气1mol,但空气中氧气只占体积分数21%,据此计算判断。
A.原电池中阴离子应该向负极移动,金属M为负极,所以电解质中的阴离子向金属M方向移动,故A错误;
B.电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,则单位质量的电极材料失去电子的物质的量越多则得到的电能越多,假设质量都是1g时,这三种金属转移电子物质的量分别为![]() ×2mol=
×2mol=![]() mol、
mol、![]() ×3mol=
×3mol=![]() mol、
mol、![]() ×2mol=
×2mol=![]() mol,所以Al空气电池的理论比能量最高,故B错误;
mol,所以Al空气电池的理论比能量最高,故B错误;
C.负极M失电子和OH反应生成M(OH)2,则正极反应式为2M-4e-+4OH-=2M(OH)2,故C正确;
D.由正极电极反应式O2+2H2O+4e=4OH有O2~4OH~4e,当外电路中转移4mol电子时,消耗氧气1mol,即22.4L(标准状况下),但空气中氧气只占体积分数21%,所以空气不止22.4L,故D错误;
故答案选C。