题目内容
硫一碘循环分解水制氢主要涉及下列反应:
Ⅰ.SO2+2H2O+I2═H2SO4+2HI
Ⅱ.2HI?H2+I2
Ⅲ.2H2SO4═2SO2+O2+2H2O
(1)整个过程中SO2、I2的作用是______.
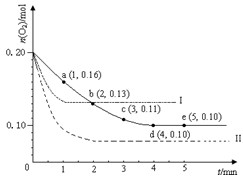
(2)一定温度下,向1L密闭容器中加入1molHI(g),发生反应Ⅱ,生成的
I2为气体,H2物质的量随时间的变化如图所示.0-2min内的平均反应速率v(HI)=______,能作为该反应达到平衡状态判断依据的是______.
①n(H2)=n(I2)
②压强不再变化
③气体密度不再变化
④2个H-I断裂的同时,有1个H-H断裂
⑤各组分浓度保持不变
⑥c(HI):c(H2):c(I2)=2:1:1
已知有关键能数据:I2-151kJ/mol、H2-436kJ/mol、HI-298kJ/mol,则分解0.2molHI时的能量变化是______(填“吸收”或“放出”)______kJ的热量.
(3)实验室用Zn和硫酸制取H2,为了加快反应速率,下列措施不可行的是(填序号)______.
a.加入浓硝酸b.加入少量CuSO4固体c.用粗锌代替纯锌d.加热e.把锌粒制成锌粉f.用98.3%浓硫酸.
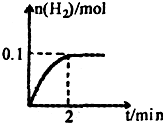
Ⅰ.SO2+2H2O+I2═H2SO4+2HI
Ⅱ.2HI?H2+I2
Ⅲ.2H2SO4═2SO2+O2+2H2O
(1)整个过程中SO2、I2的作用是______.
(2)一定温度下,向1L密闭容器中加入1molHI(g),发生反应Ⅱ,生成的
I2为气体,H2物质的量随时间的变化如图所示.0-2min内的平均反应速率v(HI)=______,能作为该反应达到平衡状态判断依据的是______.
①n(H2)=n(I2)
②压强不再变化
③气体密度不再变化
④2个H-I断裂的同时,有1个H-H断裂
⑤各组分浓度保持不变
⑥c(HI):c(H2):c(I2)=2:1:1
已知有关键能数据:I2-151kJ/mol、H2-436kJ/mol、HI-298kJ/mol,则分解0.2molHI时的能量变化是______(填“吸收”或“放出”)______kJ的热量.
(3)实验室用Zn和硫酸制取H2,为了加快反应速率,下列措施不可行的是(填序号)______.
a.加入浓硝酸b.加入少量CuSO4固体c.用粗锌代替纯锌d.加热e.把锌粒制成锌粉f.用98.3%浓硫酸.
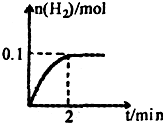
(1)SO2、I2在反应前后质量和性质不变,故答案为:催化剂;
(2)由图可知2min内氢气的物质的量增加了0.1mol,则氢气的浓度为0.1mol/L,用氢气表示的化学反应速率为
=0.05mol/(L.min),由反应中的化学计量数可知v(HI)为0.05mol/(L.min)×2=0.1mol/(L.min);①n(H2)=n(I2),没有明确反应方向,不变判断反应是否平衡;②压强自始至终不再变化,不能判断平衡;③气体自始至终密度不再变化,不能判断平衡;④2个H-I断裂的同时,有1个H-H断裂,正逆反应速率相等,能判断反应是否平衡;⑤各组分浓度保持不变是判断平衡的标志;⑥c(HI):c(H2):c(I2)=2:1:1,没有明确反应方向,不变判断反应是否平衡;根据题目中的数据,可知HI分解的反应热:△H=+298kJ/mol×2-151kJ/mol-436kJ/mol=+9kJ/mol;则分解0.2molHI需要吸收:
×0.2mol=0.9kJ,故答案为:0.1mol/L.min;④⑤;吸收;0.9;
(3)加入浓硝酸、用98.3%浓硫酸,溶液具有强氧化性,则不会生成氢气;加热、粗锌代替纯锌、把锌粒制成锌粉,都能加快反应速率;加入CuSO4后,Zn与硫酸铜溶液反应置换出Cu,则构成原电池加快了化学反应速率,故答案为:a、f.
(2)由图可知2min内氢气的物质的量增加了0.1mol,则氢气的浓度为0.1mol/L,用氢气表示的化学反应速率为
| 0.1mol/L |
| 2min |
| 9kJ/mol |
| 2 |
(3)加入浓硝酸、用98.3%浓硫酸,溶液具有强氧化性,则不会生成氢气;加热、粗锌代替纯锌、把锌粒制成锌粉,都能加快反应速率;加入CuSO4后,Zn与硫酸铜溶液反应置换出Cu,则构成原电池加快了化学反应速率,故答案为:a、f.

练习册系列答案
相关题目
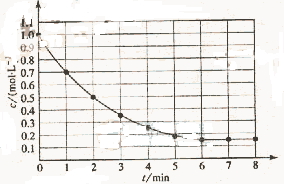
 4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线:
4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线:
 B(g)+3C(g)在下列四种状态时属于平衡状态的是( )
B(g)+3C(g)在下列四种状态时属于平衡状态的是( )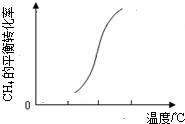 则△H2______0(填“<”、“>”或“=”).在T℃时的1L密闭容器中,充入1molCH4和3molH2O(g),发生反应②,经过5min达到平衡,此时CH4的转化率为50%,则从开始到平衡,H2的平均反应速率为______,T℃时该反应的平衡常数为______;
则△H2______0(填“<”、“>”或“=”).在T℃时的1L密闭容器中,充入1molCH4和3molH2O(g),发生反应②,经过5min达到平衡,此时CH4的转化率为50%,则从开始到平衡,H2的平均反应速率为______,T℃时该反应的平衡常数为______;