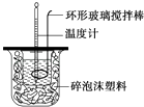
题目内容
【题目】根据图示回答下列问题:
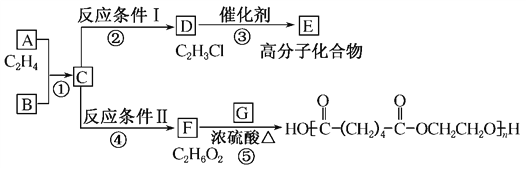
(1)写出A、E、G的结构简式:A________,E________,G________。
(2)反应②的化学方程式(包括反应条件)是_________________________,反应④的化学方程式(包括反应条件)是________________________。
(3)写出①、③、⑤的化学方程式及反应类型:
①___________________________________________________;
③___________________________________________________;
⑤___________________________________________________。
【答案】 CH2=CH2 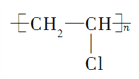 HOOC(CH2)4COOH )ClCH2CH2Cl+NaOH
HOOC(CH2)4COOH )ClCH2CH2Cl+NaOH![]() CH2=CHCl+NaCl+H2O ClCH2CH2Cl+2NaOH
CH2=CHCl+NaCl+H2O ClCH2CH2Cl+2NaOH![]() HOCH2CH2OH+2NaCl CH2=CH2+Cl2―→ClCH2CH2Cl加成反应
HOCH2CH2OH+2NaCl CH2=CH2+Cl2―→ClCH2CH2Cl加成反应 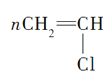
![]()
 加聚反应
加聚反应 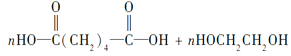
![]()
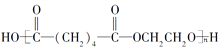 +(2n-1)H2O缩聚反应
+(2n-1)H2O缩聚反应
【解析】本题主要考查卤代烃的性质。
(1)A、E、G分别是乙烯、聚氯乙烯、己二酸,它们的结构简式:A CH2=CH2,E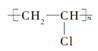 ,G HOOC(CH2)4COOH。
,G HOOC(CH2)4COOH。
(2)C是1,2-二氯乙烷,反应②发生卤代烃1,2—二氯乙烷的消去反应,反应的化学方程式(包括反应条件)是ClCH2CH2Cl+NaOH![]() CH2=CHCl+NaCl+H2O,反应④发生卤代烃1,2-二氯乙烷的水解反应,反应的化学方程式(包括反应条件)是ClCH2CH2Cl+2NaOH
CH2=CHCl+NaCl+H2O,反应④发生卤代烃1,2-二氯乙烷的水解反应,反应的化学方程式(包括反应条件)是ClCH2CH2Cl+2NaOH![]() HOCH2CH2OH+2NaCl。
HOCH2CH2OH+2NaCl。
(3)①、③、⑤的化学方程式及反应类型:
①CH2=CH2+Cl2―→ClCH2CH2Cl,加成反应,③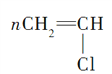
![]()
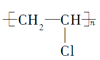 ,加聚反应,
,加聚反应,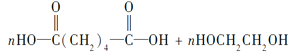
![]()
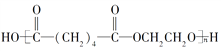 +(2n-1)H2O,缩聚反应。
+(2n-1)H2O,缩聚反应。

【题目】根据表中的信息判断下列说法正确的是( )
物质 | 金刚石 | 石墨 |
外观 | 无色,透明固体 | 灰黑,不透明固体 |
熔点 | ? | ? |
燃烧热/KJmol﹣1 | 395.4 | 393.5 |
A.表示石墨燃烧热的热化学方程式为C(石墨,s)+ ![]() ?O2(g)═CO(g)△H=﹣393.5 kJ?mol﹣1
?O2(g)═CO(g)△H=﹣393.5 kJ?mol﹣1
B.由表中信息知C(石墨,s)═C(金刚石,s)△H=+1.9 kJ?mol﹣1
C.由表中信息可得如图所示的图象 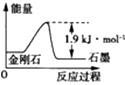
D.由表中信息可推知相同条件下金刚石的熔点高于石墨的
【题目】A,B,C,D,E,F六种化合物,其中A,B,C,D,E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成.B、C的组成元素相同,且C的摩尔质量比B大80g/mol,回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为
A.离子键
B.极性共价键
C.非极性共价键
D.氢键
(2)下表为B与F实验的部分内容
①在含B的溶液中加入稀H2SO4 , 产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
写出B与稀H2SO4反应的离子方程式
写出②中反应的化学方程式
(3)现由6种粒子Mn2+、MnO ![]() 、H+、H2O、X2Y
、H+、H2O、X2Y ![]() (C中含有的阴离子),XY
(C中含有的阴离子),XY ![]() 完成一个离子方程式,已知Mn2+为还原剂,得到1molMnO
完成一个离子方程式,已知Mn2+为还原剂,得到1molMnO ![]() 需氧化剂的物质的量为mol
需氧化剂的物质的量为mol
(4)化合物D和E相互转化D ![]() E,若有D和ExH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为g,ExH2O的化学式为 .
E,若有D和ExH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为g,ExH2O的化学式为 .