题目内容
17.下列实验操作中错误的是( )| A. | 蒸发操作时,当蒸发皿中的水分只残留少许时,停止加热,利用余热将剩余水分蒸干 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 从碘水中萃取碘时,往分液漏斗中先后加入碘水和酒精,充分静置后分液 |
分析 A.蒸发时,不能蒸干;
B.蒸馏测定馏分的温度;
C.分液时,避免上下层液体混合;
D.酒精与水互溶,不能作萃取剂.
解答 解:A.蒸发时,不能蒸干,当蒸发皿中的水只残留少许时,停止加热,利用余热将剩余水分蒸干,故A正确;
B.蒸馏测定馏分的温度,则应使温度计水银球靠近蒸馏烧瓶的支管口处,故B正确;
C.分液时,避免上下层液体混合,则应先从分液漏斗的下口放出下层液体,再从上口倒出上层液体,故C正确;
D.酒精与水互溶,不能作萃取剂,则碘水中萃取碘时,往分液漏斗中先后加入碘水和苯(或四氯化碳),充分振荡静置后分液,故D错误.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及实验基本操作和混合物分离提纯方法,注重实验技能的考查,注意实验操作的评价性分析,题目难度不大.

练习册系列答案
相关题目
7.某有机物在O2中充分燃烧,生成36g水和44g CO2,则该有机物的组成必须满足的条件是( )
| A. | 分子式一定是CH4 | B. | 分子式一定是CH4O | ||
| C. | 分子式可能是CH4或CH4O | D. | 以上说法均不正确 |
8.某无色透明溶液含有下列离子中的几种:Mg2+、Cu2+、Ba2+、H+、SO42-、OH-、NO3-、HCO3-,在其中加入金属铁,发生反应放出气体只有H2.根据上述描述判断上述离子中一定不能大量存在于此溶液中的有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
12.下列各组物质中,所含分子数不相同的是( )
| A. | 1molO2和1molH2 | B. | 5.6LN2(标准状况下)和11gCO2 | ||
| C. | 224mLH2(标准状况下)和0.1molN2 | D. | 9gH2O和0.5molBr2 |
9.下列物质一定属于同系物的是( )
① ②
② ③
③ ④C2H4⑤CH2═CH-CH═CH2⑥C3H6
④C2H4⑤CH2═CH-CH═CH2⑥C3H6
⑦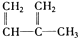 ⑧
⑧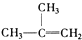
①
 ②
② ③
③ ④C2H4⑤CH2═CH-CH═CH2⑥C3H6
④C2H4⑤CH2═CH-CH═CH2⑥C3H6⑦
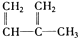 ⑧
⑧
| A. | ④和⑧ | B. | ①、②和③ | C. | ⑤和⑦ | D. | ④、⑥和⑧ |
6.1L A气体与0.5L B气体反应,恢复原温度和压强时,生成气体的体积为1L,已知生成物的化学式为X2Y,则A的分子式为( )
| A. | XY2 | B. | X3Y | C. | X2 | D. | Y2 |
7.已知反应:
①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
下列结论正确的是( )
①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
下列结论正确的是( )
| A. | 碳的燃烧热大于110.5 kJ•mol-1 | |
| B. | 2C(g)+O2(g)═2CO(g)△H>-221 kJ•mol-1 | |
| C. | 98%的浓硫酸与稀氢氧化钠溶液反应生成1mol水的中和热为-57.3kJ•mol-1 | |
| D. | 稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 |