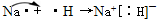题目内容
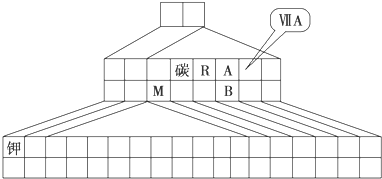
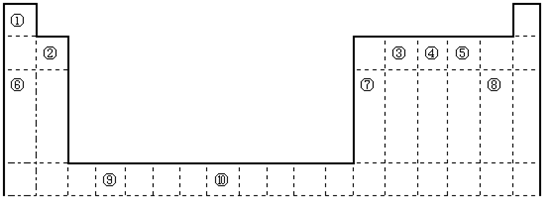
如图是元素周期表的一部分,针对表中的①---⑥短周期元素,回答下列问题
(1)最活泼的金属元素是
(2)④的原子结构示意图为:
 它在周期表中的位置为
它在周期表中的位置为
①②两元素形成的最简单化合物的电子式为

(3)②和⑤两种元素原子半径较大的是
(4)写出①的单质在⑥的单质中燃烧的化学方程式
③④两种元素的最高价氧化物对应的水合物之间可发生反应,该反应的离子方程式为:
| ① | |||||||
| ② | |||||||
| ③ | ④ | ⑤ | ⑥ |
Na
Na
(填元素符号)(2)④的原子结构示意图为:


第三周期,第ⅢA族
第三周期,第ⅢA族
①②两元素形成的最简单化合物的电子式为


(3)②和⑤两种元素原子半径较大的是
Si
Si
(填元素符号),②、⑤和⑥三种元素最高价氧化物对应的水合物酸性较强的是HClO4
HClO4
(填化学式);(4)写出①的单质在⑥的单质中燃烧的化学方程式
H2+Cl2
2HCl
| ||
H2+Cl2
2HCl
;
| ||
③④两种元素的最高价氧化物对应的水合物之间可发生反应,该反应的离子方程式为:
Al(OH)3+OH-═AlO2-+2H2O
Al(OH)3+OH-═AlO2-+2H2O
.分析:(1)元素周期表中,从上到下,金属的活泼性逐渐增强,从右到左,金属的活泼性逐渐增强;
(2)根据原子结构示意图的画法和电子式的书写方法来回答;
(3)根据元素周期律中原子半径以及最高价氧化物对应水化物酸碱性的强弱来回答;
(4)根据氯气和氢氧化铝的性质来回答.
(2)根据原子结构示意图的画法和电子式的书写方法来回答;
(3)根据元素周期律中原子半径以及最高价氧化物对应水化物酸碱性的强弱来回答;
(4)根据氯气和氢氧化铝的性质来回答.
解答:解:根据元素在周期表中的分布,可以推知①是H,②是C,③是Na,④是Al,⑤是Si,⑥是Cl.
(1)元素周期表中,从上到下,金属的活泼性逐渐增强,从右到左,金属的活泼性逐渐增强,所以最活泼的金属元素是Na,故答案为:Na;
(2)金属铝是13号元素,原子结构示意图为: ,它位于周期表的第三周期,第ⅢA族,C和H形成的最简单的化合物是甲烷,电子式为:
,它位于周期表的第三周期,第ⅢA族,C和H形成的最简单的化合物是甲烷,电子式为: ;
;
故答案为: ;第三周期,第ⅢA族;
;第三周期,第ⅢA族; ;
;
(3)同一主族从上到下,原子半径逐渐增大,所以半径:C<Si,周期表中从上到下元素最高价氧化物对应水化物的酸的酸性逐渐减弱,从左到右元素最高价氧化物对应水化物的酸的酸性逐渐增强,所以酸性最强的是HClO4,故答案为:HClO4;
(4)氢气在氯气中燃烧的化学方程式为:H2+Cl2
2HCl,氢氧化铝是两性氢氧化物,可以和强碱反应生成盐和水,即Al(OH)3+OH-═AlO2-+2H2O,
故答案为:H2+Cl2
2HCl;Al(OH)3+OH-═AlO2-+2H2O.
(1)元素周期表中,从上到下,金属的活泼性逐渐增强,从右到左,金属的活泼性逐渐增强,所以最活泼的金属元素是Na,故答案为:Na;
(2)金属铝是13号元素,原子结构示意图为:
 ,它位于周期表的第三周期,第ⅢA族,C和H形成的最简单的化合物是甲烷,电子式为:
,它位于周期表的第三周期,第ⅢA族,C和H形成的最简单的化合物是甲烷,电子式为: ;
;故答案为:
 ;第三周期,第ⅢA族;
;第三周期,第ⅢA族; ;
;(3)同一主族从上到下,原子半径逐渐增大,所以半径:C<Si,周期表中从上到下元素最高价氧化物对应水化物的酸的酸性逐渐减弱,从左到右元素最高价氧化物对应水化物的酸的酸性逐渐增强,所以酸性最强的是HClO4,故答案为:HClO4;
(4)氢气在氯气中燃烧的化学方程式为:H2+Cl2
| ||
故答案为:H2+Cl2
| ||
点评:本题是一道元素周期表结构和元素周期律知识的综合题目,考查学生分析和解决问题的能力,难度不大.

练习册系列答案
相关题目
 如图是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和为21.下列说法正确的是( )
如图是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和为21.下列说法正确的是( )| A、X元素最多可形成六种氧化物 | B、Y元素的最高价氧化物的水化物是含氧酸中酸性最强的 | C、X元素的非金属性比Y元素非金属性强 | D、Z和X能以共价键结合形成一种无机非金属材料 |