题目内容
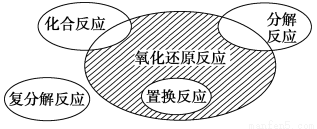
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影部分的是 ( )。
A.Cl2+2KBr=Br2+2KCl
B.2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O=4Fe(OH)3
D.2Na2O2+2CO2=2Na2CO3+O2
D
【解析】阴影部分所表示的反应类型为氧化还原反应,不属于四种基本反应类型。A为置换反应且属于氧化还原反应,不符合题意;B为分解反应,且该反应是非氧化还原反应,不符合题意;C为有单质参加的化合反应,属于氧化还原反应,不符合题意;D不属于四种基本反应类型,但属于氧化还原反应,符合题意。

 应用题作业本系列答案
应用题作业本系列答案党的十八大报告中首次提出“美丽中国”的宏伟目标。节能减排是中国转型发展的必经之路,工业生产中联合生产是实现节能减排的重要措施,下图是几种工业生产的联合生产工艺:

请回答下列问题:
(1)装置甲为电解池,根据图示转化关系可知:A为____________(填化学式),阴极反应式为____________。
(2)装置丙的反应物为Ti,而装置戊的生成物为Ti,这两个装置在该联合生产中并不矛盾,原因是_________________________________________________
装置戊进行反应时需要的环境为________(填字母序号)。
A.HCl气体氛围中 B.空气氛围中 C.氩气氛围中 D.水中
(3)装置乙中发生的是工业合成甲醇的反应:CO(g)+2H2(g)??CH3OH(g) ΔH<0。
①该反应在不同温度下的化学平衡常数(K)如下表:
温度/℃ | 250 | 350 |
K | 2.041 | x |
符合表中的平衡常数x的数值是________(填字母序号)。
A.0 B.0.012 C.32.081 D.100
②若装置乙为容积固定的密闭容器,不同时间段各物质的浓度如下表:
| c(CO) | c(H2) | c(CH3OH) |
0 min | 0.8 mol·L-1 | 1.6 mol·L-1 | 0 |
2 min | 0.6 mol·L-1 | y | 0.2 mol·L-1 |
4 min | 0.3 mol·L-1 | 0.6 mol·L-1 | 0.5 mol·L-1 |
6 min | 0.3 mol·L-1 | 0.6 mol·L-1 | 0.5 mol·L-1 |
反应从2 min到4 min之间,H2的平均反应速率为________。反应达到平衡时CO的转化率为________。反应在第2 min时改变了反应条件,改变的条件可能是________(填字母序号)。
A.使用催化剂 B.降低温度
C.增加H2的浓度
(4)装置己可以看作燃料电池,该燃料电池的负极反应式为____________ ________________________________________________。

