题目内容
【题目】如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制95mL 1mol·L-1的稀硫酸。
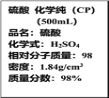
可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。
请回答下列问题:
(1)配制稀硫酸时,除玻璃棒外还缺少的仪器是__(写仪器名称);
(2)经计算,配制95mL 1mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积为__mL,量取硫酸时应选用___mL规格的量筒(填序号);
A.10mL B.50mL C.100mL D.200mL
(3)取25mL 1mol·L-1的硫酸,向其中加入一定量的氧化铜,充分反应后制得硫酸铜溶液。用该溶液制取CuSO4·5H2O,所需要的主要玻璃仪器除酒精灯、玻璃棒外,还缺少的仪器是___;
(4)对所配制的稀硫酸进行测定,发现其浓度大于1mol·L-1,配制过程中下列各项操作可能引起该误差的原因___(填序号)。
A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
C.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作
D.转移溶液时,不慎有少量溶液洒到容量瓶外面
E.定容时,俯视容量瓶刻度线进行定容
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
【答案】100mL的容量瓶 5.4 A 烧杯、漏斗 ACE
【解析】
(1)用浓硫酸配制稀硫酸的实验步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶,根据该实验步骤确定缺少的仪器;
(2)根据稀释定律:稀释前后溶质物质的量不变,计算所需浓硫酸的体积;量取硫酸时应依据“大而近”的原则选择量筒;
(3)用硫酸铜溶液制取CuSO4·5H2O,需要经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,据此判断所需仪器;
(4)根据公式![]() ,判断操作不当对于溶质物质的量、溶液体积的影响,从而判断对浓度的影响。
,判断操作不当对于溶质物质的量、溶液体积的影响,从而判断对浓度的影响。
(1)用浓硫酸配制稀硫酸的实验步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶,根据该实验步骤可知所需的仪器有:量筒、烧杯、玻璃棒、100mL容量瓶和胶头滴管,结合已知的可用仪器可知,除玻璃棒外还缺少的仪器是100mL容量瓶;
故答案为:100mL的容量瓶;
(2)根据稀释定律可知稀释前后溶质物质的量不变,则V×1.84g/cm3×98%=0.1L×1mol·L-1×98g/mol,解得V=5.4mL,量取硫酸时应选用10mL规格的量筒;
故答案为:5.4;A;
(3)用硫酸铜溶液制取CuSO4·5H2O,需要经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,则所需要的主要玻璃仪器除酒精灯、玻璃棒外,还缺少的玻璃仪器是烧杯、漏斗;
故答案为:烧杯、漏斗;
(4)A.用量筒量取浓硫酸时,仰视刻度线,量取的浓硫酸偏大,则溶质物质的量偏大,结果浓度偏大;
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水,无影响;
C.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作,未进行冷却,则加入的蒸馏水偏少,则溶液的体积偏小,造成浓度偏大;
D.转移溶液时,不慎有少量溶液洒到容量瓶外面,溶质损失,则浓度偏小;
E.定容时,俯视容量瓶刻度线进行定容,加入的蒸馏水体积偏小,则浓度偏大;
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处,加入的蒸馏水体积偏大,浓度偏小;
综上所述:ACE会使得所配置的溶液的浓度偏大;
故答案为:ACE。

 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案