题目内容
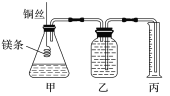
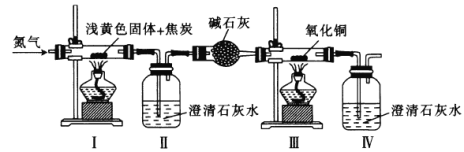
【题目】将某浅黄色固体(由X、Y两种元素组成)和焦炭混合,加热,发生反应,其装置如图所示。先通入氮气,再点燃I、Ⅲ中的酒精灯,实验中观察到I中生成银白色金属,Ⅱ、Ⅳ中溶液变浑浊、Ⅲ中黑色粉末变成红色。下列叙述不正确的是
A.X可能是钠元素,Y一定是氧元素
B.浅黄色固体与焦炭在高温下反应生成CO2和CO
C.先通入氮气的目的是排尽装置中的空气
D.用燃烧法处理Ⅳ排放的尾气
【答案】A
【解析】
根据实验现象可知,淡黄色固体为过氧化钠,加热时碳与过氧化钠反应生成一氧化碳、二氧化碳,则装置II溶液变浑浊,碱石灰吸收二氧化碳,一氧化碳与氧化铜反应生成二氧化碳,装置IV溶液变浑浊。
A.分析可知,淡黄色物质为过氧化钠,X是钠元素,Y是氧元素,A错误;
B.根据实验现象,浅黄色固体与焦炭在高温下反应生成CO2和CO,B正确;
C.装置中的空气会影响实验结论,则先通入氮气的目的是排尽装置中的空气,C正确;
D.尾气中含有未反应的CO,则用燃烧法处理Ⅳ排放的尾气,D正确;
答案为A。

练习册系列答案
相关题目