题目内容
已知100℃时,0.01mol·L-1 NaHSO4溶液中水电离的c(H+) =10-10 mol·L-1,该温度下将pH=8的Ba(OH)2溶液V1 L与pH=5 V2 L NaHSO4混合,所得溶液pH=7,则 V1∶V2=
A.2∶9 B.1∶9 C.1∶1 D.1∶2
【答案】
A
【解析】0.01mol·L-1 NaHSO4溶液中水电离的c(H+) =10-10 mol·L-1,说明溶液中OH-的浓度也是10-10 mol·L-1,氢离子浓度是0.01mol/L,所以该温度下水的离子积常数为1×10-12。所得溶液pH=7,说明溶液显碱性,即碱是过量的,所以有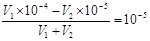 ,解得V1∶V2=2∶9,答案选A。
,解得V1∶V2=2∶9,答案选A。

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目